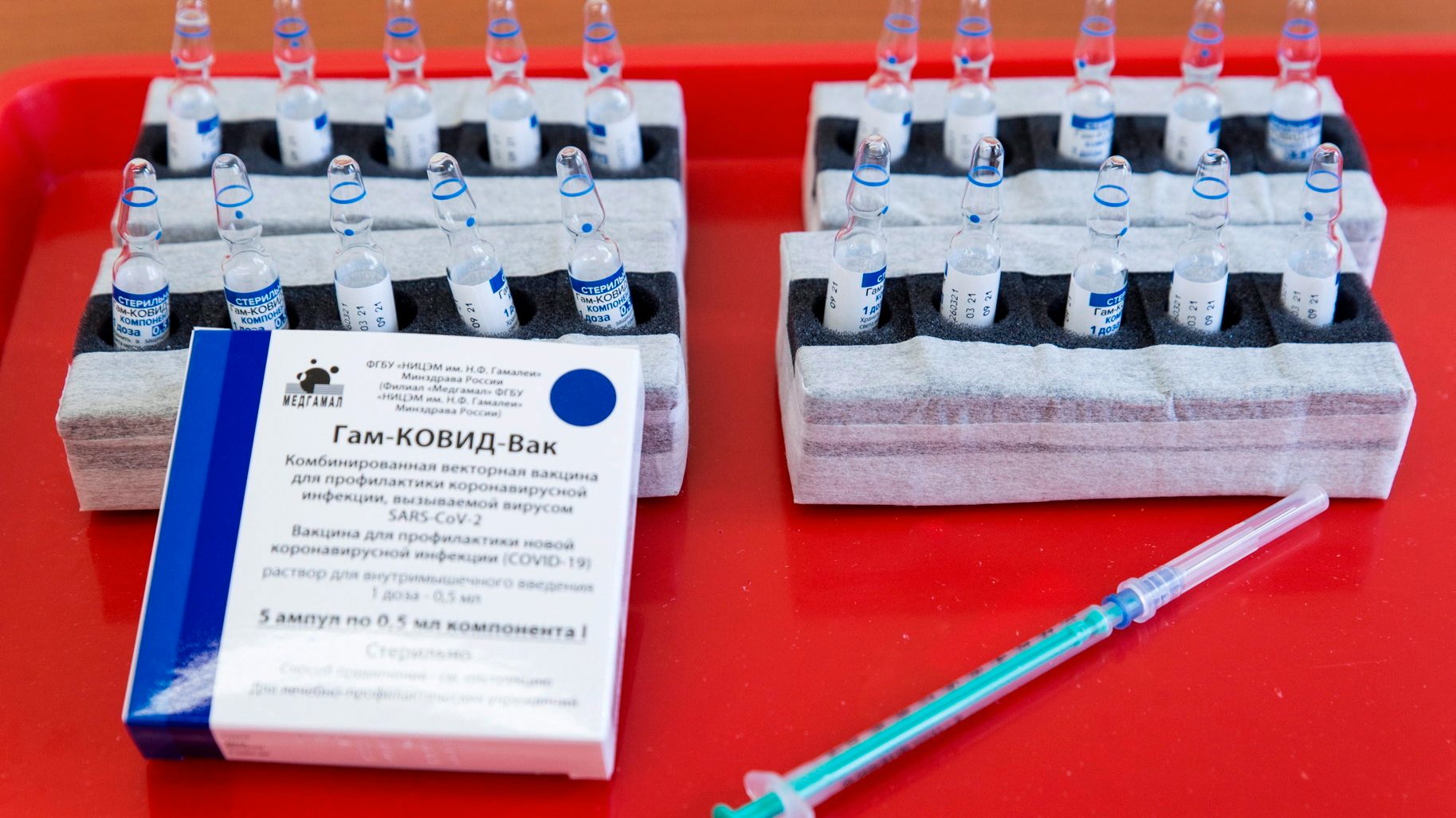
A agência reguladora brasileira Anvisa recusou esta segunda-feira a vacina russa Sputnik V por considerar existirem falhas no desenvolvimento e na produção do imunizante, lê-se no comunicado publicado no portal do Governo. A Agência Nacional de Vigilância Sanitária (Anvisa) diz mesmo que se verifica uma “falta de dados consistentes e confiáveis” sobre o imunizante pelo que, após reunião colegial, decidiu recusar a sua aquisição.
Na Europa, a EMA decidiu investigar os testes clínicos da Sputnik V.
“Espero que, de fato, o processo da vacina Sputnik V adeque as suas informações e resolva rapidamente as questões de conformidade, porque milhões de pessoas precisam ter acesso a vacinas seguras e eficazes”, disse a diretora Meiruze Freitas após a decisão, que lembrou que a Anvisa está “a fazer tudo” para “garantir que as vacinas para a Covid-19 cheguem às pessoas desta nação e que atendam aos padrões de qualidade, segurança e eficácia”.
Segundo o comunicado, as várias equipas técnicas da Anvisa encontraram falhas no desenvolvimento da vacina em todas as etapas dos estudos clínicos (fases 1, 2 e 3). E debateram-se com falta de informações no controlo de qualidade, segurança e eficácia.
Em contraponto, Denis Logunov, o principal responsável da Sputnik V, diz que cada lote da vacina passa por um rigoroso processo de análise, como conta a Reuters, citada pelo The Guardian. “A vacina é limpa […] e não contém adenovírus competentes para replicação”, disse Logunov a jornalistas. Logunov referiu ainda que a injeção passou por um processo de limpeza e filtração de quatro fases e isso é raro entre os fabricantes de vacinas, afirma.
Uma das informações que mais preocupou o regulador foi o facto de as células onde os adenovírus são produzidos para o desenvolvimento da vacina permitirem a sua replicação. “Isso pode acarretar infeções em seres humanos, podendo causar danos e óbitos, especialmente em pessoas com baixa imunidade e problemas respiratórios, entre outros problemas de saúde”, lê-se no comunicado. Um efeito que, dizem ainda estes peritos, “foge dos padrões de qualidade” recomendados pela Organização Mundial da Saúde (OMS) e pelo Conselho Internacional para Harmonização de Requisitos Técnicos de Medicamentos para Uso Humano (International Council for Harmonisation of Technical Requirements for Pharmaceuticals for Human Use – ICH).
Também os estudos de caracterização da vacina, incluindo a análise de impurezas e de vírus contaminantes durante o processo de fabricação, foram considerados “inadequados”. E mais uma vez a falta de informação sobre quais os métodos de controlo de qualidade e o registo de testes de toxicidade reprodutiva — que permitem verificar se o produto pode ou não ser prejudicial às células reprodutivas.
O regulador chama também a atenção para a questão do desconhecimento de efeitos secundários da vacina a curto, médio e longo prazo.
A Diretoria Colegiada da Anvisa, reunida nesta segunda, decidiu não autorizar a importação da vacina Sputnik V. Técnicos da Agência apresentaram análises que apontam inconsistências nos dados disponíveis até o momento sobre o imunizante. Leia mais em: https://t.co/oSlAS3XSny pic.twitter.com/wIagy8EkPV
— Anvisa (@anvisa_oficial) April 27, 2021
Já a equipa da fiscalização, que chegou mesmo a ir à Rússia para uma missão de inspeção, debateu-se com a mesma falta de informações. No terreno, não obteve qualquer relatório técnico de aprovação do produto, não conseguiu identificar os fabricantes do produto farmacêutico biológico utilizado na produção da vacina russa, assim como as condições da sua produção. Mais, quando tentou aceder às instalações do Gamaleya, o instituto que está a desenvolver vacina na Rússia, e viu o acesso ser-lhe barrado.
Foram 14 os estados brasileiros que pediram a importação desta vacina: Acre, Alagoas, Amapá, Bahia, Ceará, Maranhão, Mato Grosso, Pará, Pernambuco, Piauí, Rio Grande do Norte, Rondônia, Sergipe e Tocantins, além dos municípios fluminenses de Maricá e Niterói.
À Globo, o relator da decisão, Alex Machado Campos, classificou a situação atual desta vacina como um “mar de incertezas” e diz que dados apurados apontam um cenário de riscos “impressionante”.
A Agência Europeia de Medicamentos (EMA) anunciou há dias que vai investigar os testes clínicos da vacina russa Sputnik V para perceber se respeitaram de facto os padrões científicos e éticos apropriados.
Covid-19. Agência Europeia do Medicamento vai investigar se ensaios da Sputnik V respeitaram padrões
No início do mês, o secretário de Estado para os Assuntos Europeus francês, Clément Beaune, afirmou que a vacina russa contra a Covid-19 Sputnik V não devia estar autorizada na UE antes do final de junho. Ainda assim ela é já usada em vários países.
Entre os 27 Estados-membros da União Europeia, apenas a Hungria, Eslováquia e República Checa decidiram até agora usar a vacina russa, optando por não esperar pela validação por parte da EMA. Mas há países na América Latina que já a administram.
O responsável pelo Fundo russo de investimento direto, Kirill Dmitriev, tem vindo a público defender a vacina e referiu que os reguladores dos 59 países já aprovaram o Sputnik V, depois de verificaram todos os dados com o rigor exigido.
Hungria será o primeiro país da UE a usar a vacina russa Sputnik V
*Notícia atualizada às 19h57 com resposta do responsável russo da vacina Sputnik V.