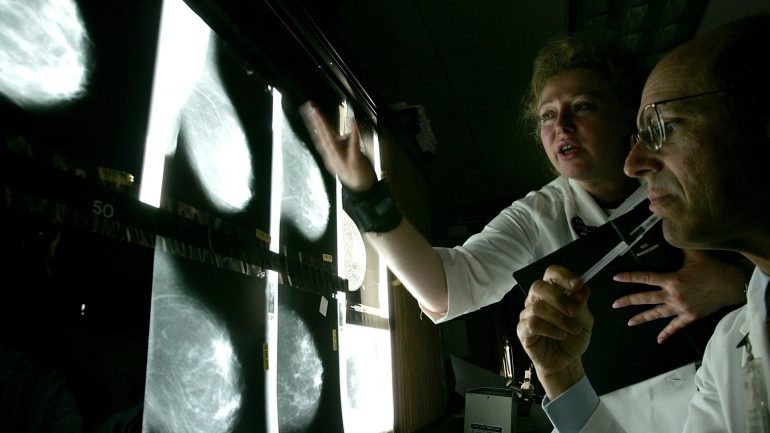
A quimioterapia continua a ser o tratamento mais comum no combate ao cancro – ainda que possa ser combinado com outras terapias. Mas apesar da eficácia, este tratamento não está livre de efeitos secundários severos, a médio e longo prazo. E se fosse possível reduzir o número de mulheres que fazem quimioterapia para tratar o cancro da mama? Essa era a ideia de Fátima Cardoso, diretora da Unidade de Cancro da Mama, no Centro Clínico Champalimaud (Lisboa), quando iniciou o projeto Mindact. As conclusões foram publicadas na passada semana na revista científica The New England Journal of Medicine.
↓ Mostrar
↑ Esconder
Eliminar tratamentos amplamente aceites e que têm um resultado positivo no tratamento de uma doença é um desafio, lembram Clifford A. Hudis e Maura Dickler, autores do editorial deste número da revista.
Os investigadores concluíram que 46% das mulheres, com cancro da mama em estádio inicial, que são classificadas como doentes de alto risco pelos métodos tradicionais podem evitar fazer quimioterapia. A novidade é a utilização de um teste genético para avaliar este risco. Não que os testes genéticos em si sejam novos, mas o que a equipa internacional, da qual Fátima Cardoso fazia parte, fez foi validar a utilização de um teste com ensaios clínicos, como se faz sempre que se prepara um novo medicamento para entrar no mercado.
Os testes genéticos já existem no mercado há algum tempo, mas a falta de validação para a utilidade dos testes tem deixado profissionais de saúde e doentes confusos quanto ao caminho a seguir. Daí que haja uma “pressão sobre a FDA [Food and Drug Administration] e a EMA [Agência Europeia do Medicamento] para criarem regras para as firmas que produzem estes testes”, diz a investigadora ao Observador.
O cancro da mama é o segundo tipo de cancro mais comum em todo o mundo.
Com estes resultados, os investigadores validaram o teste baseado em 70 genes da empresa Agendia – o Mammaprint. Esta análise não pretende identificar os genes que estão presentes ou ausentes, como a sequenciação genética costuma fazer, mas pretende identificar que genes estão ativos ou inativos no tumor. “Diferentes expressões [ativo ou inativo], representam diferentes funções”, explica a investigadora ao Observador.
Assim, esta “assinatura genómica” do tumor (a avaliação da atividade dos genes) tem um “valor de prognóstico” – bom ou mau prognóstico –, explica a oncologista. Isto quer dizer que para mulheres com um bom prognóstico, ou seja, com uma probabilidade de sobrevida superior a 95%, a vantagem da quimioterapia é muito baixa. As mulheres com mau prognóstico têm um risco de recidiva de 50%. Mas nuns e noutros casos, a decisão final (depois de devidamente informada sobre riscos e vantagens), quanto à realização da quimioterapia, é da mulher.
O teste pode ser usado em todos os casos de cancro da mama?
Embora Fátima Cardoso veja vantagem neste teste genético, porque considera que existe atualmente um sobretratamento do cancro da mama, também alerta que a análise não será útil para todas as mulheres e que para algumas será sempre recomendado que façam quimioterapia.
O primeiro requisito é que o cancro da mama esteja num estádio inicial, podendo ter no máximo um a três nódulos na axila. Não poderá ter metástases, para que seja potencialmente curável. Os tumores muito grandes – mesmo que não sejam muito agressivos –, os cancros com células tumorais agressivas – mesmo que sejam pequenos –, e os casos em que existem metástases, estão todos recomendados para fazer quimioterapia. Logo o teste genético torna-se desnecessário.
Depois é preciso definir subtipo de cancro da mama: se está relacionado com a proteína HER2, se está relacionado com as hormonas ou se não é nenhum dos casos anteriores (triplonegativo). Os tumores relacionados com a proteína HER2 são normalmente muito agressivos e, embora exista tratamento específico para este tipo de cancros, a quimioterapia é sempre usada como um tratamento adjuvante. Nestes casos, mesmo com teste genético, seria impossível, à luz do conhecimento atual, descartar a quimioterapia. Para o triplonegativo, como não tem nenhum tratamento específico, a quimioterapia é a única possibilidade disponível, logo o teste genético também não tem interesse nestes casos.
Uma em cada oito mulheres pode vir a receber um diagnóstico de cancro da mama.
O subtipo de cancro da mama que está dependente das hormonas é o mais frequente, afetando dois terços das mulheres que sofrem desta doença. E é exatamente para este tipo de cancro que identificar a assinatura genómica se torna mais útil. A hormonoterapia é o tratamento mais eficaz para este subtipo de cancro, mas, consoante o grau de risco de reaparecimento do cancro, pode ser recomendada a quimioterapia como tratamento adjuvante.
O risco de recidiva era tradicionalmente definido em termos clínico-patológicos – neste estudo recorreu-se à ferramenta Adjuvant!Online –, como pelo tamanho do tumor, o número de gânglios linfáticos afetados, a agressividades das células tumorais, o perfil hormonal e a idade da mulher, entre outros parâmetros. Neste estudo, as mais de 6.600 mulheres tiveram o risco clínico e genómico (pelo teste genético) avaliado e uma de três situações poderia acontecer: ambas as análises identificavam um baixo risco, logo não era preciso recorrer à quimioterapia; ambas as análises identificavam um risco alto, logo as mulheres eram recomendadas a seguir um tratamento com quimioterapia; ou as análises davam riscos discordantes – um alto e outro baixo.
Se a avaliação de risco clínico dá um resultado muito diferente da avaliação de risco genómico, qual deve ser seguido? Também aqui existem duas situações possíveis com duas respostas diferentes. Fátima Cardoso conta que tiveram algumas situações em que o risco clínico era baixo, mas o risco genómico era alto. Contudo, como o número de doentes nesta situação era muito baixo, não conseguiram ter dados que lhes permitissem tirar conclusões estatisticamente significativas.
Em 2010, cerca de um milhão de pessoas, incluindo 10 mil homens, foram diagnosticados com cancro da mama.
Já para os casos em que o risco clínico era identificado como alto, mas o risco genómico era identificado como baixo (1.550 mulheres), os investigadores verificaram que não seria preciso recorrer à quimioterapia para evitar o reaparecimento do cancro. O estudo concluiu que 95% das doentes estavam, ao fim de cinco anos, livres de metástases, independentemente de terem feito quimioterapia ou não.
“Não podemos concluir que o benefício da quimioterapia [nestes casos] seja zero, mas é muito pequeno – cerca de 1,5%”, diz Fátima Cardoso. “Por 1,5% valerá a pena os efeitos secundários a médio e longo prazo?” A investigadora não se refere às náuseas ou queda de cabelo, comuns a quem está a fazer o tratamento, mas aos problemas cardíacos e outros tumores que podem surgir mais tarde. A preocupação dos médicos é ainda maior quando se tratam de mulheres jovens, porque podem viver tempo suficiente para que estes efeitos secundários mais graves se manifestem.
De qualquer forma, e como lembram Clifford A. Hudis e Maura Dickler do Memorial Sloan Kettering Cancer Center, “uma diferença de 1,5 pontos percentuais, se real, pode significar mais para um doente do que para outro”. Fátima Cardoso reforça que embora os médicos possam fornecer a melhor informação disponível, a decisão cabe aos doentes.
Como é que decorreu este trabalho de investigação?
Este trabalho começou há 10 anos, conta Fátima Cardoso, porque as doentes foram acompanhadas, e a informação recolhida, desde o momento do teste genético até ao aparecimento (ou não) da recidiva. Por isso, e para ter dados que permitam tirar conclusões válidas, é preciso que os estudos sejam prolongados no tempo. “O cancro da mama pode voltar mesmo 20 anos depois”, diz a médica. Daí que a equipa envolvida neste trabalho dê continuidade ao trabalho de acompanhamento das doentes, pelo menos, durante 10 anos.
Existem muitos testes no mercado, mas nenhum deles está validado com ensaios clínicos. “Há menos controlo na disponibilização dos testes antes de estarem validados cientificamente”, refere a investigadora. Este é o primeiro teste genético deste tipo a ter um ensaio clínico publicado. Há outro ensaio clínico em curso, mas os resultados ainda não estão publicados. “Utilizados com sabedoria, [estes testes] permitem diminuir custos com a quimioterapia e os custos indiretos (deixar de trabalhar, despesas com deslocações).”
Para levar um teste genético a ensaios clínicos, que concluíram agora a fase III, a equipa escolheu o Mammaprint, porque tem uma assinatura genómica robusta. A empresa fornecedora do teste e as empresas farmacêuticas que fabricam os medicamentos para a quimioterapia terão apoiado este trabalho, mas não terão tido nenhuma influência no desenvolvimento do trabalho científico.
O trabalho contou com a participação de 6.693 doentes com cancro da mama – entre os 18 e os 70 anos –, recrutadas entre 2007 e 2011 de 112 hospitais, pertencentes a nove países europeus (nenhum dos hospitais era português). Todas as participantes foram avaliadas para o risco clínico e risco genómico e, nos casos em que o risco clínico era alto e o risco genómico baixo, as doentes foram distribuídas aleatoriamente por dois grupos: um que foi sujeito a quimioterapia e outro que não.
Este trabalho de investigação foi financiado em 47 milhões de euros.