Os antibióticos são a arma mais poderosa para combater as infeções bacterianas. Pelo menos, depois da infeção estar instalada. Mas o uso de antibióticos também tem um lado negro: além de potenciarem o desenvolvimento de bactérias multirresistentes, também modificam — talvez irreversivelmente — as bactérias que vivem no nosso organismo.
“O lado negro dos antibióticos” foi precisamente o tema que Carlos Úbeda, investigador no Centro Superior de Investigação em Saúde Pública (em Valência, Espanha), trouxe às 11ª Jornadas de Atualização em Doenças Infecciosas do Hospital de Curry Cabral.
A visão sobre as bactérias tem-se alterado ao longo do tempo: dos germes que temos de eliminar a todo o custo, às bactérias que cumprem funções importantes no nosso organismo. A investigação científica tem permitido descobrir que as bactérias podem ajudar a digerir alguns alimentos, que podem contribuir para o desenvolvimento do nosso sistema imunitário e do nosso sistema nervoso e que até podem contribuir para a prevenção de doenças.
Bactérias boas e bactérias más
↓ Mostrar
↑ Esconder
Bactérias comensais são bactérias que vivem no nosso organismo. Estas bactérias obtêm benefícios, podem conferir alguns benefícios ao hospedeiro e não os prejudicam.
Bactérias patogénicas são aquelas que nos causam doenças.
Bactérias multirresistentes são bactérias que se tornaram resistentes a dois ou mais antibióticos.
O grupo de investigação de Carlos Úbeda está focado na capacidade de as bactérias comensais conferirem proteção contra patogenos multirresistentes e nos mecanismos que usam para o fazer. Conhecer melhor esta forma de proteção pode ajudar a criar terapias alternativas aos antibióticos.
As experiências realizadas até agora, mostraram à equipa de Valência que os antibióticos interferem na composição da flora intestinal — quantidade e variedade — e que mesmo depois de se parar de tomar os antibióticos, o microbiota não recuperou a composição inicial. Neste processo, as bactérias multirresistentes podem sobreviver. Havendo menos bactérias comensais para lhes fazer frente, acabam por colonizar o intestino e tornar ainda mais difícil a sua eliminação.

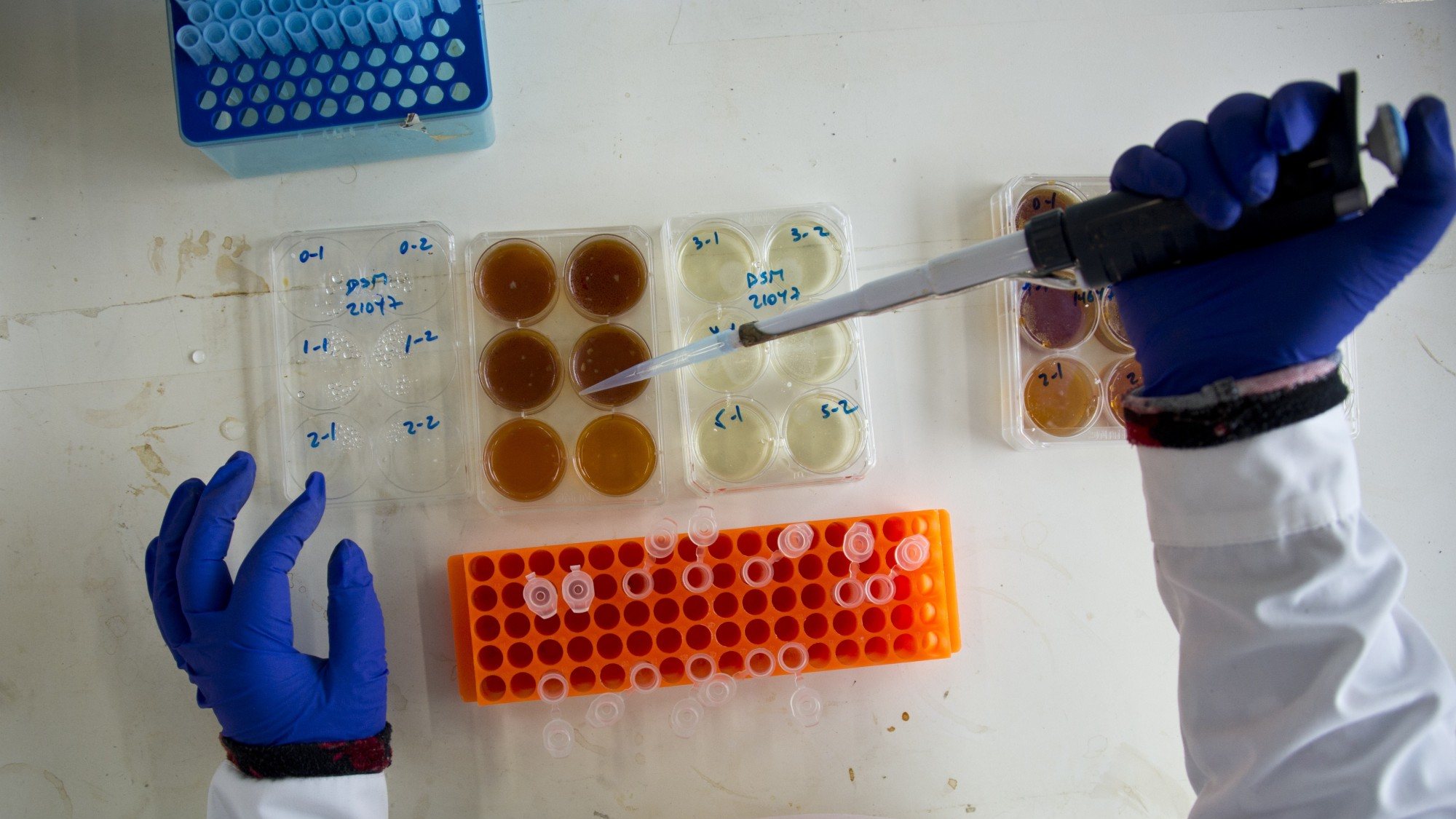
▲ Carlos Úbeda e a equipa do Centro Superior de Investigação em Saúde Pública, em Valência, querem perceber como é que as bactérias comensais evitam a colonização de bactérias patogénicas
Vera Novais/Observador
O que há de errado com os antibióticos? Qual é o “lado negro”?
Sabemos que os antibióticos são vantajosos, no sentido em que graças a eles temos conseguido lutar contra as infeções, mas o lado mau é que os antibióticos alteram o microbiota, as bactérias que temos — principalmente nos nossos intestinos, mas também noutras partes do nosso organismo. Os antibióticos também matam estas bactérias e, porque alteram o microbiota, acabam por promover infeções por patogenos resistentes. Em condições normais, o nosso microbiota confere-nos proteção, mas quando o perturbamos com os antibióticos, alguns patogenos que antes não eram capazes de colonizar o trato intestinal, são capazes de o fazer. A partir daqui, podem disseminar-se por outras partes do corpo. Este é o lado mau dos antibióticos, vão alterar o nosso microbiota.
Há alguma maneira de combater as bactérias patogénicas sem usar antibióticos?
Atualmente, a forma de combater bactérias patogénicas é com antibióticos. Mas há antibióticos de diferentes espectros, portanto, uma das coisas que tem sido proposta para combater as bactérias sem alterar o microbiota é usar antibióticos tão restritos quanto possível. Neste sentido, alguns trabalhos de investigação identificaram que há peptídeos que afetam algumas bactérias, logo não vão matá-las todas, vão ter um espectro mais reduzido. É mais dirigido ao patogeno, em vez de afetar qualquer tipo de bactéria e alterar o microbiota.
Estamos a tentar perceber de que forma o microbiota confere proteção contra os patogenos. Dentro desses mecanismos [de proteção, usados pelas bactérias comensais] existem alguns envolvidos na indução da resposta imunitária, outros na competição por nutrientes e outros ainda envolvidos na produção de moléculas inibidoras, como os peptídeos de que falei. Compreender e identificar estes mecanismos vai permitir-nos criar novas terapêuticas que são uma alternativa aos tratamentos com antibióticos.
Tem resultados sobre esses tipos de mecanismos?
Em geral, sabe-se que algumas bactérias comensais vão produzir moléculas inibidoras que impedem o crescimento de alguns patogenos. Há trabalho feito em relação à competição por nutrientes específicos, visto que há algumas bactérias comensais, que ocupam o mesmo nicho que o patogeno, a usar o mesmo tipo de nutrientes. Logo, o patogeno não consegue crescer. Também há trabalho feito sobre bactérias comensais específicas que vão induzir as respostas imunitárias e permitir a eliminação do patogeno. A resposta imunitária implica ativação das células T e produção de peptídeos antimicrobianos, que vão ajudar a remover o patogeno.
Probióticos e prébióticos
↓ Mostrar
↑ Esconder
Os probióticos são microorganismos que vivem no intestino. Ajudam na digestão e protegem o organismo contra as bactérias nocivas. Também podem ser encontradas em iogurtes e leites fermentados, como o Kefir, e o ideal é que cheguem ao intestino vivos.
Os prébióticos estimulam o crescimento e atividade das bactérias probióticas. Como são hidratos de carbono não digeríveis (fibra) servem de alimento para os probióticos. Estão presentes na cevada, aveia, trigo, bananas, cebolas, alho, alho-francês, mel ou alcachofras.
Está a falar de medicamentos que podem potenciar a ação destas bactérias comensais?
Nem sequer precisamos de falar de medicamentos, podemos falar de nutrientes, prébióticos, que são os nutrientes que as bactérias vão usar, logo, que vão potenciar o crescimento de bactérias benéficas. Outro tipo de abordagem pode ser dar esse tipo de bactérias como probióticos. Outra estratégica pode ser identificar as moléculas que as bactérias comensais produzem para ativar o sistema imunitário ou para reprimir diretamente as bactérias patogénicas. Podemos tentar sintetizar essas moléculas ou purificá-las para as usar diretamente como agente terapêutico.
Para as bactérias comensais conseguirem combater as bactérias patogénicas têm de ser mais fortes. Mas mesmo sem o uso de antibióticos podem não ser mais fortes.
Normalmente são, pelo menos para o tipo de patogenos que estudo: Enterococcus multirresistente ou Enterobacteriaceae multirresistente — que são resistentes a múltiplos antibióticos. Em condições normais, numa pessoa saudável, que tenha um microbiota próximo da normalidade, sem grandes perturbações, os patogenos não são capazes de colonizar o intestino. Porque o microbiota é capaz de prevenir a colonização. Só em certas situações, quando o microbiota está alterado, como em doentes hospitalizados a receber tratamentos com antibióticos orais, estas bactérias patogénicas serão capazes de colonizar o intestino.
Além dos antibióticos, há mais algum fator que possa perturbar o microbiota?
A dieta é um fator importante na alteração do microbiota. Há vários trabalhos de investigação — a maior parte em ratos — que mostraram claramente que a dieta ocidental — rica em açúcares simples, pobre em fibra e rica em gordura — altera a composição do microbiota e promove doenças, como obesidade e diabetes. A dieta é um fator importante. Há alguns trabalhos que mostram que o hospedeiro também pode moldar o microbiota: o sistema imunitário também é importante para condicionar a composição do microbiota.
Quando o microbiota sofre alterações ficamos mais expostos às doenças, além das infeções?
Sim, exatamente. Tem sido feitos uma série de trabalhos de investigação em humanos que tentam correlacionar mudanças no microbiota com doenças. O microbiota influencia a obesidade. Numa experiência, retiraram o microbiota de ratos obesos e colocaram-no em ratos livres de germes (“germ free mice”, que não têm qualquer bactéria). Estes ratos tiveram maior tendência para se tornarem obesos do que os ratos que receberam o microbiota de ratos esguios. Ambos os ratos receberam a mesma dieta. Fizeram alguns ensaios e parece que o microbiota dos obesos é mais eficiente a recolher a energia dos alimentos. Foi por isso que os ratos se tornaram obesos com a mesma dieta.
Para o cancro colorretal, há trabalhos que associam a presença de uma bactéria em particular — Fusobacterium — com a incidência de cancro colorretal. Há observações em ratos que mostram que esta bactéria, pelo menos em alguns passos, promove o desenvolvimento do cancro.
É uma bactéria que faz parte do microbiota normal?
É difícil dizer o que é um microbiota normal. Mas sim, é uma bactéria que costuma estar presente. O que demonstraram é que a sua presença era mais relevante nos doentes que desenvolveram este tipo de cancro. E a investigação que fizeram associava a presença desta bactéria com o cancro.
O que quero dizer sobre ser normal ou não é que, como pode imaginar, além de ter esta bactéria, a pessoa terá de ter, enquanto hospedeiro, alguma predisposição para desenvolver a doença. A presença da bactéria num determinado indivíduo poderá não ser prejudicial, ou mesmo benéfica, mas noutro indivíduo poderá ser nociva. Acho que podemos dizer que a bactéria mais saudável é aquela que, independentemente do hospedeiro, não vai causar nenhum malefício, só trará vantagens.
As bactérias, em geral, até podem ser benéficas, mas se se desenvolverem demais podem tornar-se potencialmente patogénicas. Mesmo que não se tornem patogénicas, a diversidade do microbiota vai diminuir e podemos ter, mesmo assim, efeitos prejudiciais, porque se uma aumentou outra diminuiu. Essencialmente, para termos um estado saudável precisamos de um microbiota diversificado, sem predominância de uma bactéria e sem a presença de bactérias que estejam associadas a doenças ou que promovam doenças.
Que características do microbiota são ainda pouco conhecidas?
A ideia de que as bactérias são más está a mudar completamente. Na última década têm sido feitos muitos trabalhos com o microbiota. Agora apercebemo-nos de que estas bactérias têm vivido connosco desde há milhares de anos, co-evoluíram connosco. Foram importantes para o desenvolvimento do sistema imunitário e para o desenvolvimento do sistema neuronal. Não sei se as pessoas têm noção da complexidade que existe dentro do nosso intestino. Há estudos que dizem que cada pessoa tem entre 100 e 1000 espécies diferentes só no intestino. E quando falamos em números de bactérias temos centenas de milhares de milhão de bactérias no intestino.
Sem falar no número de genes. Os genes têm a capacidade de produzir proteínas. E estes excedem em muito o número de genes que temos no nosso corpo. Isto significa que nos fornecem funções que não temos. Algumas pessoas consideram que é como outro órgão no nosso corpo, que é necessário para algumas funções que não somos capazes de realizar sozinhos. Uma função típica é a digestão de alguns componentes dos alimentos. Mas agora sabemos muito mais sobre o desenvolvimento do sistema imunitário, sobre o desenvolvimento do sistema nervoso e sobre a proteção contra patogenos.