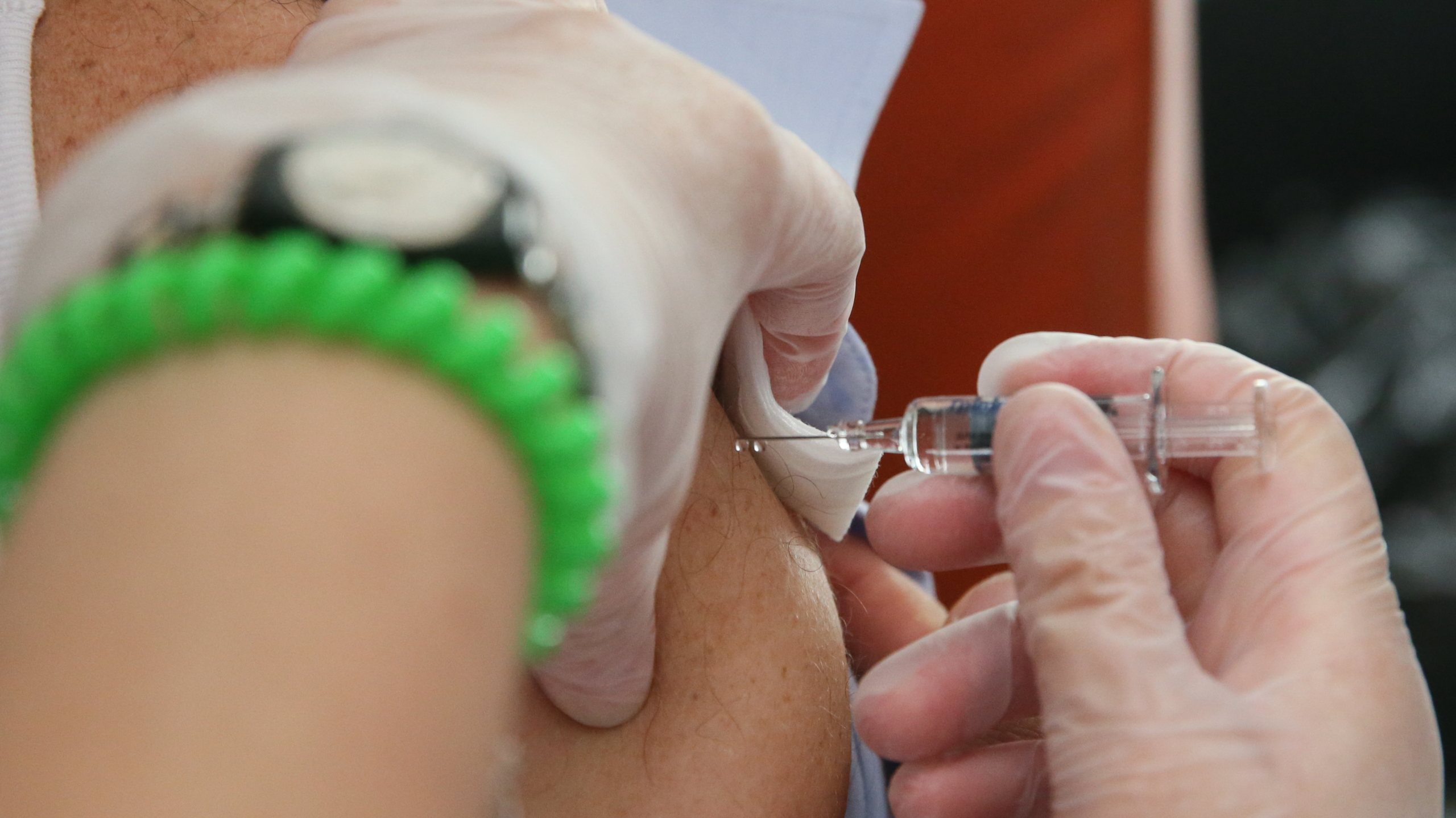
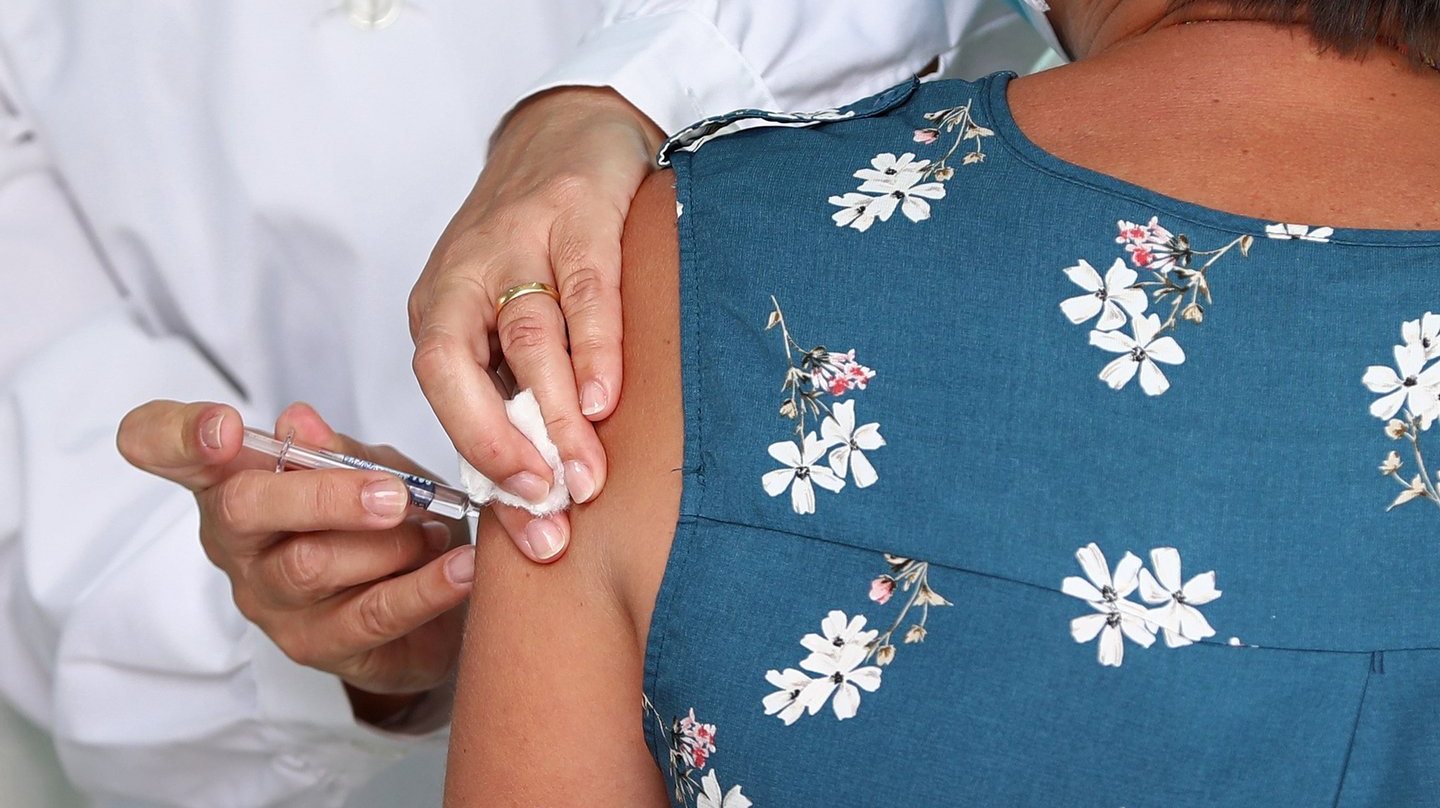
Uma análise feita pela agência norte-americana do medicamento (Food and Drug Administration, FDA na sigla inglesa) à vacina produzida pela Pfizer e pela BioNTech contra a Covid-19 confirmou a sua eficácia e segurança, mas esta ainda não é a aprovação final da vacina.
A notícia é avançada pelos jornais norte-americanos Washington Post e New York Times, que citam documentos publicados esta terça-feira pela FDA. Os cientistas que pertencem à FDA passaram as últimas duas semanas a analisar os dados da Pfizer e chegaram às mesmas conclusões: a vacina tem uma eficácia de 95% e os efeitos adversos, como dores de cabeça, dores de corpo, cansaço e febre, acabam por desaparecer ao fim de um a dois dias, refere o Washington Post.
Os dados de segurança relativos a 38 mil participantes no ensaio clínico da vacina, que tiveram um acompanhamento clínico médio de dois meses, “sugerem um perfil de segurança favorável”, já que não foi identificado um problema específico de segurança que impeça a autorização de emergência, referem os especialistas.
A vacina oferece “uma forte proteção” contra o novo coronavírus cerca de 10 dias após a toma da primeira dose da vacina e funcionou em diversas pessoas independentemente da idade, sexo, peso e etnia, explica o New York Times. A vacina também resultou em pessoas obesas. Falta também apurar a duração da imunidade da vacina.
Notaram-se alguns efeitos adversos na toma da vacina em vários participantes. Os mais comuns, registados nos 43.252 participantes, incluindo crianças e adolescentes com 12 anos ou mais, foram: reação tópica junto ao local de imunização (braço) (84,1%), fadiga (62,9%), dor de cabeça (55,1%), dores no corpo (38,3%), calafrios (31,9%), dores nas articulações (23,6%) e febre (14,2%). Reações graves ocorreram apenas em zero a 4,6% dos participantes e foram menos comuns em pessoas com mais de 55 anos (2,8%) do que em jovens (4,6%).
A FDA refere, contudo, que não se notaram grande diferenças entre as pessoas que foram vacinadas e as que tomaram um placebo no que toca aos efeitos adversos. Ainda assim, houve quatro pessoas a quem foi administrada a vacina que tiveram uma espécie de paralisia facial (paralisia de Bell), lê-se no New York Times.
As reações adversas graves — como, por exemplo, as que obrigaram a hospitalização – foram muito raras ao longo do ensaio clínico (menos de 0,5%) e registaram-se tanto nos imunizados com placebo como nos que receberam a vacina, o que leva a concluir que esta não esteja em causa. Os efeitos adversos menos graves são mais comuns em pessoas com menos de 55 anos, o que poderá dever-se ao sistema imunológico das pessoas mais jovens ser mais ativo.
Este relatório trouxe, porém, um elemento novo no que toca à eficácia da vacina, sugerindo que esta não é apenas eficaz para formas graves de infeção pelo novo coronavírus, após as duas inoculações, como também o é na prevenção da doença após a toma da primeira dose. O estudo demonstra também eficácia nas pessoas que tinham sido infetadas antes pelo novo coronavírus, mas sublinha que estas não podem ser tomadas ainda como “conclusões definitivas”.
Recorde-se que a Pfizer anunciou em meados de novembro que a vacina, produzida em parceria com a alemã BioNTech, tinha 95% de eficácia e que iria pedir uma Autorização de Uso de Emergência ao regulador americano. A luz verde está por dias — deverá acontecer até ao final da semana —, mas ainda não foi desta.
Vacina da Pfizer com 95% de eficácia. Farmacêutica vai pedir aprovação de emergência
Estes documentos serão analisados por um painel de conselheiros da FDA na próxima quinta-feira que irão decidir se recomendam ou não a autorização da vacina. Independentemente da aprovação, as farmacêuticas vão continuar a acompanhar os participantes dos ensaios para garantir que eficácia e segurança da vacina a longo prazo.