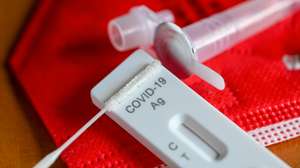
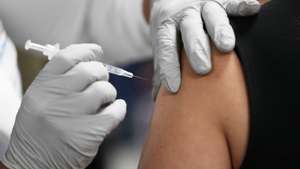
A decisão da Agência Europeia do Medicamento (EMA) sobre a administração da vacina contra a Covid-19 da Pfizer/BioNTech em crianças entre os 5 e os 11 anos apenas deve ser conhecida no final do ano.
“A proposta assenta numa dose três vezes mais baixa do que a dose aprovada para adultos. O calendário proposto para esta administração é de manter as duas doses separadas por pelo menos três semanas. A nossa recomendação é esperada dentro de dois meses, mas informação ou análise suplementar poderá ser necessária”, afirmou o responsável da instituição para a Estratégia de Ameaças Biológicas para a Saúde e Vacinas, Marco Cavaleri.
O prazo para o anúncio de uma recomendação sobre esta vacina (Comirnaty) surgiu numa conferência de imprensa realizada esta quinta-feira em Amesterdão, nos Países Baixos, apenas três dias depois de a EMA ter revelado o arranque do processo de avaliação da administração da vacina neste grupo etário. Até agora, a utilização da vacina da Pfizer/BioNTech está somente autorizada para pessoas com pelo menos 12 anos de idade.
Paralelamente, Marco Cavaleri adiantou também que estão a ser gerados dados sobre a vacinação contra a Covid-19 em crianças entre os 5 e os 11 anos para a vacina Spikevax (Moderna) e que a EMA “está a discutir o potencial timing de candidatura para a administração no futuro”, antecipando mais informações sobre este tema nas próximas semanas.
A Covid-19 provocou pelo menos 4.910.200 mortes em todo o mundo, entre mais de 241,48 milhões infeções pelo novo coronavírus registadas desde o início da pandemia, segundo o mais recente balanço da agência France-Presse.