Helder Maiato recorda-se bem dos dois momentos em que decidiu que seria a Biologia a mantê-lo na idade dos porquês. Até lá, admite, “o coração esteve dividido entre as artes e a ciência”, até porque, ao tentar encontrar uma explicação para o interesse nos dois caminhos, constata que “são vertentes criativas, de exploração, de insatisfação”.
Como sempre teve destreza para desenhar decidiu, no nono ano, “experimentar” estudar Artes. Passou um ano a fazer esboços de moda e, apesar de ter aprendido técnicas que hoje ainda usa, detestou a experiência. No ano seguinte, enveredaria pelo curso de Quimicotecnia, constatando que gostava mais de desenhar problemas científicos – e procurar respostas para eles.
O segundo momento foi quando o cientista do Instituto de Investigação e Inovação em Saúde (i3S), no Porto, era escuteiro e se envolveu num episódio em que “tudo o que poderia correr mal, correu mal”. O seu grupo foi fazer um raide noturno, no pico do inverno, na Serra da Freita, concelho de Arouca. Já em plena montanha, a 1100 metros de altitude, foram apanhados por uma tempestade. Chovia torrencialmente. Não tinham como escapar à intempérie. Tentaram abrigar-se. “Montamos uma tenda, mas a água era tanta que, a meio da noite, começou a entrar e ficamos encharcados.” Para piorar a situação, formou-se um riacho por baixo da tenda. Tiveram de, madrugada adentro, encontrar uma solução. Caminharam até à aldeia mais próxima para pedir abrigo. “Alguém tinha uma casa que estava a construir, sem janelas, sem portas, sem nada, mas com paredes e telhado. No dia seguinte, depois da tempestade, acordamos em plena Serra da Freita e estava tudo branco. Tinha nevado de noite e ainda estava a nevar”. Ato contínuo, deu-se o clique. “Este contacto com os elementos, a proximidade com a natureza, que aliás o escutismo transmite, foi fundamental. E aí eu pensei: é a Biologia.”

Aos 45 anos, Helder Maiato é o líder do grupo de investigação do i3S (Porto) que quer descodificar o código da diversidade das tubulinas e dos microtúbulos das nossas células e assim compreender o impacto que têm na formação de metástases e na resistência aos medicamentos contra o cancro
Hoje, com 45 anos, Helder Maiato é o líder do grupo de investigação do i3S que quer descodificar o código da diversidade das tubulinas e dos microtúbulos das nossas células e assim compreender o impacto que têm na formação de metástases e na resistência aos medicamentos contra o cancro, que são atualmente dois dos grandes desafios para melhorar a sobrevivência do doente. Da sua equipa participam neste projeto António Pereira, Danilo Lopes, Liam Cheeseman, Joana Monteiro e Hugo Girão, assim como os colegas do i3S Salomé Pinho, Joana Parede, Fernando Schmitt, “entre outros colaboradores internacionais”, nomeadamente dos EUA e França.
Nas nossas células temos uma espécie de esqueleto. Chama-se citoesqueleto e parte dele é formado por umas estruturas, que se chamam microtúbulos, que são fundamentais para formar o fuso mitótico, que é o que permite a divisão dos cromossomas durante a divisão celular.”
Para melhor esclarecer a que se refere, o cientista nascido em Matosinhos roda a cadeira em que está sentado no gabinete em direção ao computador e aponta para o ecrã para mostrar pequenos filmes deste mundo microscópico. Arregala os olhos verdes, entusiasmado, e desliza o dedo indicador por uma imagem de pequenos filamentos em movimento. “Isto é a divisão celular: são os vários cromossomas a separar no momento da mitose. É este o processo que nós trabalhamos. E os tais tubos estão ligados aos cromossomas”. Para verem os microtúbulos, precisam de microscópios de alta resolução, sabemos.
A importância da divisão celular
Mas, afinal, por que razão este processo de separação é tão importante para a saúde humana? O cientista sorri com o olhar. “Primeiro, para estarmos aqui, precisamos dele. Nós derivamos de uma única célula, que deu origem a triliões de células que compõem um organismo adulto. Portanto, se não houvesse divisão celular éramos leveduras condenadas à morte”, explicita. “Então, isto assegura aquilo que designamos por homeostasia celular: o equilíbrio de todo o nosso corpo, pois há biliões de células que morrem todos os dias e que são renovadas através do processo da divisão celular.”
O nosso organismo depende da divisão de células para funcionar bem. Quando este processo falha, “sobretudo devido a erros na segregação dos cromossomas”, origina doenças. “Esta perda ou ganho de cromossomas é a característica mais transversal a todos os tipos de cancro que se conhecem.”

“Tem de ser, também, a partir do estudo da fisiologia que temos de compreender aquilo que acontece normalmente nas nossas células, nos nossos organismos, nos nossos sistemas”, diz o investigador, que quer ir à raiz do problema e não incidir a análise apenas na reação do organismo à doença
Até há bem pouco tempo, os cientistas pensavam que os microtúbulos eram todos iguais. “São diferentes”, atesta o investigador. “Como existe um código genético, que cria variedade, variabilidade e proteínas diferentes, os microtúbulos têm, também, um código – que não é genético, mas antes um código de modificações que acontecem depois de eles serem feitos e que são chamadas de modificações pós-traducionais.”
Sabe-se que essas modificações criam diversidade com diferentes propriedades e “pensamos que podem estar envolvidas na resistência a determinados fármacos”. Aliás, “muitos dos atuais fármacos contra o cancro, ao estarem dirigidos aos microtúbulos, interferem na divisão, migração e invasão celular”, especifica.
A existência dessas modificações era já conhecida há quarenta anos. “Nós não sabíamos era para o que elas serviam”, ressalva. Por isso, Helder e a equipa começaram a fazer perguntas e a levantar hipóteses.
Ter esse conhecimento que havia de facto estas modificações e não sabíamos para o que elas serviam ajudou. Eu só precisei da pergunta certa: Por que é que eu tenho aqui um cromossoma, e como é que ele ‘sabe’ que tem que ir para ali e não para lá? Como é que ele ‘sabe’ quais são as pistas que deve usar?” Até que conjeturou: “se calhar, estas modificações dos microtúbulos são usadas pelos cromossomas, para lhes indicarem o caminho.”
Helder é um apaixonado pela investigação fundamental. Na mesa ao lado da secretária tem três pilhas de artigos científicos: lidos e por ler. Serão, pelo menos, mais de cinco mil páginas empilhadas. O cientista entusiasma-se com o reparo. “Tenho ali mais três caixas com o meu arquivo. É que sou à moda antiga. Sou do papel, embora imprima menos, mas tenho um arquivo que nenhuma biblioteca do mundo tem sobre a divisão celular”. Depois, aponta para as estantes ao redor. “Aliás, toda esta parte aqui são clássicos: este livro é de 1890 e qualquer coisa, estes três têm mais de cem anos, porque, nesta altura, já se investigava sobre a divisão celular.”

Em parceria com o Hospital de São João, no Porto, a equipa de Helder Maiato terá acesso a um banco de tumores oncológicos. “Vamos tentar perceber o que se passa, para validar os resultados que temos in vitro e, depois, compreender como podemos alterar essas características”
Um dos livros seminais do século XIX que sobressai das estantes foi comprado online. “Usei-o muito; estamos a falar de uma geração [de cientistas] que não tinham os instrumentos, mas tinha a capacidade [intelectual] e muitas destas noções e ideias, já estão expostas no papel há mais de cem anos. A grande diferença é que hoje temos mais meios.”
Investigação fundamental: a raiz da árvore
O investigador do i3S insiste na importância do pensamento e da problematização constante da investigação clássica. “A nossa matriz, a nossa forma de estar, não é de todo a de aplicar a ciência, aplicar o conhecimento. Nós esperamos que o nosso conhecimento seja aplicado por outros. Estamos muito bem a trabalhar ao nível da raiz da árvore, ao nível da investigação fundamental, de conhecer, compreender. E, para chegar a este ponto, tudo começou com uma ideia que não fazia sentido nenhum à partida, mas fazia todo o sentido para nós e mais ninguém a viu e nós testamos essa ideia.”
O biólogo celular sempre foi um aluno curioso e com notas exemplares. Reconhece que não estudava muito, pois nunca foi “um aluno marrão”, mas “retinha facilmente a informação”. Talvez por isso insurge-se contra o sistema de ensino atual. “A escola tem um problema grave: está demasiado estabelecida”, começa por apontar, criticando o método de “debitar conhecimento”.

O nosso organismo depende da divisão de células para funcionar bem. Quando este processo falha, origina doenças. “Esta perda ou ganho de cromossomas é a característica mais transversal a todos os tipos de cancro que se conhecem.”
Pai de dois filhos, dá um exemplo próximo: “Eu continuo a ficar pasmado quando vejo a minha filha de 13 anos a ter que decorar coisas e depois tem extrema dificuldade em interpretar.” Esse método, acredita, “mata a curiosidade” das crianças que se tornarão adultos “resignados”, ou que “não têm o espírito crítico para questionar e para levantar dúvidas”.
É também por isso que co-fundou, em 2015, um projeto de educação de ciência nas escolas para crianças, a Yscience, para fomentar o questionamento de base e disseminar o método científico. “Trabalhamos com escolas públicas e privadas e temos cientistas que, semanalmente, de uma forma integrada no próprio currículo das ciências, estão em articulação com o professor titular da turma.”
Nós provocamos as crianças com a frase: ‘venham de lá essas perguntas sobre, obviamente, os temas que estão a aprender no currículo’. Depois tentamos desenhar uma experiência que as ajuda a concretizar, porque muitas destas noções são abstratas ainda para elas. Ajudamo-las, com as suas mãozinhas, a alimentar o espírito curioso e crítico.”
Foi esse mesmo espírito, admite, que o levou mais longe. Sendo bom aluno tinha notas altas para competir em cursos que, à partida, ofereciam saídas profissionais mais “seguras” do que a investigação científica, como a área médica. Neste quesito, o também professor universitário no departamento de Biomedicina da Faculdade de Medicina da Universidade do Porto realça o papel fundamental dos pais nas escolhas de carreira. “Eles são de origens humildes, de uma classe trabalhadora, e poderiam ter-me colocado alguma pressão para enveredar por um curso que me trouxesse outro retorno financeiro, mas nunca caíram na tentação de dizer [para seguir determinado curso]. Às vezes, o não fazer é fazer muito: é dar liberdade”.

“Se não houvesse divisão celular éramos leveduras condenadas à morte. Isto assegura o que designamos por homeostasia celular: o equilíbrio de todo o nosso corpo, pois há biliões de células que morrem todos os dias e que são renovadas através do processo da divisão celular”
Essa liberdade levou-o, em linha reta, para uma carreira científica de prestígio. É um dos especialistas mundiais no campo de mitose [uma das fazes do processo de divisão celular, em que o ADN do núcleo das células se transforma em cromossomas que são divididos pelas duas células filhas], foi conselheiro do Primeiro Ministro para a Ciência e a Tecnologia, entre 2012 e 2015, e soma já duas dezenas de prémios, entre os quais o The Louis-Jeantet Young Investigator Career Award e o Prémio de Excelência Científica da Universidade do Porto.
Helder Maiato licenciou-se em 1998 em Bioquímica na Universidade do Porto, foi aluno do concorrido programa doutoral em Biologia e Medicina da Gulbenkian (1999), doutorou-se em 2003 pelo Instituto de Ciências Biomédicas Abel Salazar (Universidade do Porto), com passagem pelos Laboratórios do Professor Claudio E. Sunkel, no Instituto de Biologia Molecular e Celular (Porto) e do Professor William C. Earnshaw, no Wellcome Trust Centre for Cell Biology, da Universidade de Edimburgo. Realizou o pós-doutoramento entre 2003 e 2004, no Wadsworth Center, no departamento de Medicina Molecular do estado de Nova Iorque.
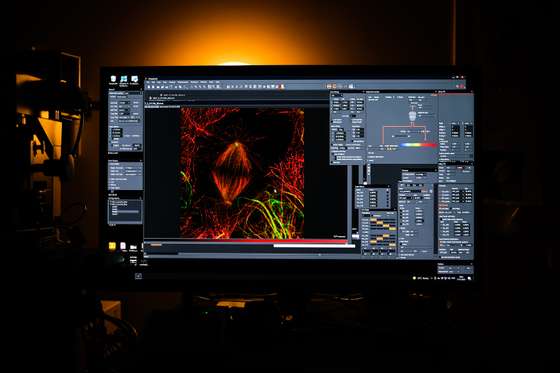
Durante a divisão celular, há um “caos inicial” e os cromossomas migram para o centro da célula. “E como é que eles sabem onde é o centro? Porque é que eles vão para ali em 99,999% dos casos?”, indaga o biólogo celular.
Entre 2017 e 2018 desfrutou de uma licença sabática que incluiu um mês e meio no Whitehead Institute (laboratório associado do prestigiado MIT, Massachusetts Institute of Technology) e no Laboratório de Biologia Marinha em Woods Hole (EUA). “É dos laboratórios de investigação mais antigos nos Estados Unidos, com uma dinâmica espetacular no Verão, reunindo investigadores de vários lugares. Foi lá que, através da Biologia Marinha se fizeram importantes descobertas a nível celular.”
“Como a descoberta das ciclinas, por exemplo, a proteína fluorescente verde que é hoje usada em microscopia. Ou a descoberta das cinesinas, proteínas importantes no transporte intracelular.” Neste laboratório internacional – a que o cientista volta sempre que pode – reforçou o espírito de comunidade e de networking.
O “código da estrada” dentro das células
Foi com esse mesmo sentido de partilha e de colaboração que, em equipa, chegaram à elaboração do projeto financiado pela Fundação “la Caixa”. A comunidade científica sabia já que, durante a divisão celular, há “um caos inicial e tudo evolui para alguma ordem”, por isso “os nossos cromossomas antes de segregarem para duas células-filhas têm de migrar para o centro da célula”. Daí a pergunta seminal deste campo: “E como é que eles sabem onde é o centro? Porque é que eles vão para ali em 99,999% dos casos?”, indaga o biólogo celular.
Em 2013, ainda tinham várias hipóteses para tentar explicar essa questão, até que chegaram a uma outra que fez mais sentido: a diversidade dos microtúbulos e a existência de uma espécie de código de estrada dentro das células.

Helder Maiato co-fundou, em 2015, um projeto de educação de ciência nas escolas para crianças, para fomentar o questionamento de base e disseminar o método científico. “Temos cientistas que, de forma integrada no currículo das ciências, estão em articulação com o professor titular da turma”
Tal traduziu-se numa descoberta fundamental, recorda, publicada, em 2015, na revista Science, num artigo que, em seis anos, tem já quase duzentas citações. “Teve grande impacto porque respondeu a uma pergunta fundamental: ‘porque é que os cromossomas têm que ir para lá?’ Porque se não forem há problemas [que podem ter implicações para o funcionamento do nosso organismo].” E são esses problemas que continuaram a investigar, uma vez que essa descoberta mudou a forma como se entende o movimento dos cromossomas durante a divisão celular.
Essa diversidade dos microtúbulos vem de um código chamado Tubulina, “que é o tijolo, a unidade básica dos microtúbulos”. A equipa liderada por Helder Maiato foi tentar perceber se essa diversidade do código estava alterada em sessenta tipos de cancro, a partir do painel de células cancerígenas NCI 60 do National Cancer Institute (EUA), onde se testam muitos dos fármacos que chegam até nós para tratamento de tumores malignos. Veredicto da investigação: “havia imensas alterações e isto ajudou-nos a perceber que estes mecanismos poderiam estar desregulados em cancro”. Essa descoberta foi em grande parte realizada “por um aluno de doutoramento, o Danilo Lopes, que veio de Cabo Verde, a propósito de um programa financiado pela Gulbenkian”.
Tratamentos personalizados contra o cancro
Agora, o que Helder Maiato e a sua equipa pretendem perceber com este novo projeto financiado em 500 mil euros pela Fundação “la caixa”, iniciado em dezembro e com a duração de três anos, é “de que forma estas alterações do código têm implicações nas propriedades que conhecemos em cancros humanos”.
Parte-se de um problema de divisão celular e chega-se a um problema de compreender por que razão as células cancerígenas fazem metástases e porque é que elas migram para outros sítios? Porque é que as células cancerígenas resistem aos fármacos?”
Logo, sendo os microtúbulos um alvo terapêutico de excelência, “será que esta diversidade de alguma forma está envolvida na resposta terapêutica que um paciente vai ter quando é exposto a este tratamento?” Isso porque “as alterações do código da tubulina parecem estar efetivamente envolvidas na resistência de vários cancros ao tratamento por algum destes fármacos.”
O foco deste projeto assenta numa visão particular que Helder tem sobre a investigação em saúde: ir à raiz potencial do problema e não incidir a análise somente na reação do organismo à doença. “Tem de ser, também, a partir do estudo da fisiologia que temos de compreender aquilo que acontece normalmente nas nossas células, nos nossos organismos, nos nossos sistemas.”

O objetivo do estudo, no limite, é fornecer dados para a medicina personalizada. Para, no futuro, se poder dizer a um paciente: “Vai fazer esta terapia e, com um grau de certeza grande, ela vai funcionar em si. Não vamos sujeitá-lo a uma terapia com efeitos secundários sérios e que, com grande probabilidade, não irá tratar o seu cancro”
Para isso, vão testar como podem manipular o código em modelos animais, para verificar o respetivo impacto fisiológico. Depois, em parceria com o Hospital de São João, no Porto, vão ter acesso a um banco de tumores oncológicos. “Trata-se de material primário de pacientes que têm determinadas características e vamos tentar perceber o que se passa, para validar os resultados que temos in vitro e, depois, compreender como podemos alterar essas mesmas características.” Para o efeito, têm também ao dispor uma tecnologia adaptada pelo físico António Pereira, o qual fez uma modificação ótica à microscopia de alta resolução – STED [stimulated emission depletion] – para permitir melhorar a visualização dos microtúbulos do fuso mitótico. “Conseguimos ver com muita nitidez essas modificações com elevada resolução, o que nos permite mapeá-las, quer num contexto normal, quer num contexto de cancro.”
O estudo desse material, enfatiza o cientista, tem como objetivo fornecer dados para a medicina personalizada. “Vai permitir, no futuro, eventualmente, intervir ao nível destes pacientes quando eles estão sujeitos a uma determinada terapia. Ou pelo menos ajudar a dizer: ‘Olhe, vai fazer esta terapia e, com um grau de certeza grande, ela vai funcionar em si. Não vamos sujeitá-lo a uma terapia que tem efeitos secundários sérios e que, com grande probabilidade, não irá tratar o seu cancro’.”
Este artigo faz parte de uma série sobre investigação científica de ponta e é uma parceria entre o Observador, a Fundação “la Caixa” e o BPI. O projeto Cracking the Cancer Tubulin Code for Precision Oncology, liderado por Helder Maiato, do i3S, foi um dos 30 selecionados (12 em Portugal) – entre 644 candidaturas – para financiamento pela fundação sediada em Barcelona, ao abrigo da edição de 2021 do Concurso Health Research. O investigador recebeu 500 mil euros para desenvolver o projeto ao longo de três anos. O concurso chama-se agora CaixaResearch de Investigação em Saúde e as candidaturas para a edição de 2022 encerram a 25 de novembro.


















