- O que é resistência antimicrobiana?
- Como é que as bactérias se tornam resistentes?
- Como prevenir o aparecimento de estirpes resistentes?
- Quais as consequências para a saúde humana?
- O que é que aquilo que comemos tem a ver com tudo isto?
- Que bactérias resistentes estão entre as que requerem mais atenção?
- O que é o problema crescente da Klebsiella pneumoniae?
- Qual é o ponto de situação em Portugal?
- O que é que os profissionais de saúde podem fazer?
- A indústria farmacêutica faz parte da solução ou do problema?
- Que contributos pode dar a comunidade científica?
Explicador
- O que é resistência antimicrobiana?
- Como é que as bactérias se tornam resistentes?
- Como prevenir o aparecimento de estirpes resistentes?
- Quais as consequências para a saúde humana?
- O que é que aquilo que comemos tem a ver com tudo isto?
- Que bactérias resistentes estão entre as que requerem mais atenção?
- O que é o problema crescente da Klebsiella pneumoniae?
- Qual é o ponto de situação em Portugal?
- O que é que os profissionais de saúde podem fazer?
- A indústria farmacêutica faz parte da solução ou do problema?
- Que contributos pode dar a comunidade científica?
Explicador
O que é resistência antimicrobiana?
De forma geral, a resistência antimicrobiana (AMR, na sigla em inglês) significa que os medicamentos usados para combater um determinado tipo de agente patogénico, como bactérias, vírus ou outros parasitas, deixaram de ser eficazes para o eliminar ou até para impedir que se multiplique na presença desse antimicrobiano. O foco, neste momento, está sobretudo na resistência das bactérias aos antibióticos (e assim será abordada neste artigo).
Os profissionais que trabalham na área dos antibióticos e da resistência crescente das bactérias aos vários tipos de antibióticos são unânimes: a AMR constitui atualmente um dos maiores desafios no que diz respeito à saúde pública. Mas apesar de ser reconhecida como um problema urgente, nem todos os países têm planos para a combater. E este não é um problema apenas dos países desenvolvidos, como lembra a Organização Mundial de Saúde (OMS), já foi detetada em todas as partes do mundo e os relatórios de várias regiões demonstram que está a aumentar.
[jwplatform lB8O1APz]
Desde que começaram a ser usados, nos anos 40, os antibióticos demonstraram que podiam tornar-se ineficazes se as bactérias desenvolvessem resistência contra eles, mas acreditava-se que seria possível arranjar sempre novas drogas. Só nos anos 80, quando começaram a aparecer as primeiras estirpes de bactérias resistentes a vários tipos de antibióticos, se começou a perceber que o problema poderia ser maior do que o inicialmente previsto.
A resistência antimicrobiana não é um problema apenas para as pessoas que tomaram demasiados antibióticos ou que adquiriram bactérias resistentes de outras formas, mas para todas as pessoas que as rodeiam que podem ser infetadas com essas bactérias que vão deixar descendência resistente ou partilhar esta informação genética a outras bactérias.
Conoce las causas de la resistencia a los #antibióticos https://t.co/BkBELo6ndI #AntibioticResistance pic.twitter.com/nCrDk6vbHI
— World Health Organization (WHO) (@WHO) November 11, 2015
Basta lembrar o caso recente da bactéria no Centro Hospitalar de Vila Nova de Gaia/Espinho que contaminou mais de 30 pessoas desde agosto. As suspeitas recaem sobre uma doente que fez vários ciclos de antibiótico e que, no dia 29 de julho, esteve na mesma unidade de pós-operatório que o primeiro paciente infetado. E segundo afirmou o diretor-geral da Saúde, Francisco George, a origem do problema foi o uso indevido de antibióticos.
Como é que as bactérias se tornam resistentes?
A primeira ideia que deve ser esclarecida é que são as bactérias que se tornam resistentes aos antibióticos e não as pessoas. Se o tratamento com antibióticos não está a surtir o efeito desejado num doente, significa que este medicamento não está a conseguir eliminar ou impedir a propagação das bactérias que causaram a doença.
A segunda é que a resistência antimicrobiana é um processo natural, mas que, neste caso, o aparecimento e a disseminação está a ser potenciado pelo uso incorreto de antibióticos e pela ausência de regulamentação sobre a sua utilização, pela falta ou ineficácia de programas de controlo e prevenção de infeções, pela má qualidade dos medicamentos usados ou pela vigilância insuficiente.
As bactérias são microrganismos unicelulares que evoluem rapidamente porque uma mutação num gene pode facilmente originar uma nova estirpe dessa bactéria. Este gene mutado pode conferir características muito distintas das que possuía a bactéria original, incluindo sobreviver a um agente agressor, como um antibiótico. Além disso, as bactérias podem facilmente adquirir material genético de outras bactérias e assim tornarem-se também elas resistentes sem ser por hereditariedade genética.
How does #AntibioticResistance spread? New infographic by @ECDC_EU ahead of #EAAD 2015 pic.twitter.com/Jw7YHCIsRe
— Camille Perrin (@Perrin_Cam) November 12, 2015
Um antibiótico atua matando (ou inibindo a atuação) as bactérias. Bem, quase todas, na melhor das hipóteses. As que sobrevivem podem propagar-se, essencialmente por dois mecanismos. Por um lado, se um antibiótico não as conseguiu vencer da primeira vez, muito provavelmente não conseguirá à segunda tentativa, logo é preciso mudar de antibiótico. Por outro, como as outras comunidades de bactérias foram eliminadas, as bactérias mais resistentes podem replicar-se sem encontrarem oposição de outras populações de bactérias.
Normalmente, o crescimento das populações de bactérias é controlado pelas outras bactérias presentes. Como as bactérias comunicam umas com outras bactérias através de vários compostos, alguns deles com características antimicrobianas, perceber como estes compostos funcionam pode ser uma via para aprender a controlar o crescimento destas comunidades de microrganismos.
Para explicar este tema a miúdos e graúdos, o Centro Ciência Viva de Sintra criou a exposição “Resistir: quando as bactérias sobrevivem aos antibióticos” e uma banda desenhada (que pode ser descarregada aqui).
Como prevenir o aparecimento de estirpes resistentes?
Os antibióticos, também chamados de antibacterianos, servem exclusivamente para tratar infeções causadas por bactérias, logo não deve ser usado para tratar constipações ou gripes, porque estas são causadas por vírus. Parece uma situação lógica, mas é um dos casos mais comuns de mau uso de antibióticos. Além disso, usar antibióticos de forma inapropriada pode ter consequências negativas imediatas, como diarreia, vómitos e erupções cutâneas.
Assim, não insista com o médico para lhe receitar um antibiótico se não tem a certeza que tem uma infeção com uma bactéria. Do outro lado, o lado dos médicos, não se devem sentir pressionados pelos doentes para prescrever um antibiótico só porque o doente exige uma solução para o problema. “Todos nós temos de fazer a nossa parte para melhorar a situação”, disse ao Observador Andrea Ammon, diretora do ECDC.
- 50% dos antibióticos prescritos nos hospitais e 45% prescritos nos consultórios, nos Estados Unidos, são para doenças que não podem ser tratadas com antibióticos.
- 80% dos antibióticos usados nos Estados Unidos são para os animais de criação.
Mark your calendar: Join our World Antibiotics Awareness Week Tweet Chat, Nov 18 10am ET Qs w/ #AntibioticResistance pic.twitter.com/ZrD27xyd8G
— PAHO/WHO (@pahowho) November 11, 2015
“Se não posso tomar antibióticos, o que posso fazer?”
Aconselhe-se com o médico sobre que medicamentos podem aliviar os sintomas, como febre ou dores de cabeça; beba muitos líquidos e fique em repouso durante uns dias – não é à toa que se diz que devemos ficar de cama, é a forma do organismo se concentrar em combater a doença; e vacine-se. Embora as vacinas sejam sobretudo para doenças causadas por vírus, o facto de reduzir a probabilidade de ter uma destas infeções também vai diminuir as idas ao médico e a possibilidade de tomar antibióticos indevidamente.
Campanha para o Dia Europeu da Sensibilização para os Antibióticos de 2009 – ECDC
Lembre-se da importância de ter cuidados de higiene: lavar as mãos sempre que usa os lavabos, que espirra ou se assoa ou quando as mãos estão visivelmente sujas; antes de comer ou beber e de tocar das feridas; e, no caso dos doentes ou visitantes num hospital, antes de entrar e sair do quarto.
Não se automedique. Não deve guardar antibiótico para tomar noutra altura, nem tomar um antibiótico que sobrou e foi prescrito noutra situação; não deve tomar um medicamento sugerido por um familiar ou amigo, nem fazer sugestões de medicamentos aos conhecidos. Por sua vez, o médico deve garantir que a infeção é causada por uma bactéria (e qual) de forma a ajustar o tipo de antibiótico, a dosagem e a duração do tratamento.
We support @WHO 1st World #Antibiotic Awareness Week 16-22.11 #AntibioticResistance #EU https://t.co/mh5hSf7zi3 pic.twitter.com/iapSGmzah3
— EU One Health (@EU_Health) November 10, 2015
Outros erros comuns são:
- Aconselhar o antibiótico mais forte quando um mais fraco seria suficiente ou aconselhar um antibiótico mais fraco quando era necessário atacar a infeção de uma forma mais agressiva e eficaz;
- Escolher um antibiótico generalista em vez de utilizar um antibiótico mais específico para a bactéria em causa;
- Manter um tratamento com antibióticos durante demasiado tempo.
Quais as consequências para a saúde humana?
As infeções por bactérias resistentes aos antibióticos são responsáveis pelo aumento da morbilidade e mortalidade, bem como pelo prolongamento do internamento hospitalar, alerta o ECDC. Encontrar uma terapia eficaz pode demorar mais tempo, quando se está perante uma bactéria resistente, causando infeções cada vez mais graves e podendo levar à morte do doente antes de ser encontrada a melhor solução.
“Tratar um paciente com tuberculose resistente, por exemplo, custa o mesmo que tratar 100 pacientes com tuberculose não resistente”, disse Swarup Sarkar, diretor do Departamento de Doenças Contagiosas do escritório regional do Sudeste Asiático da Organização Mundial de Saúde (OMS).
As bactérias resistentes são responsáveis por 25 mil mortes humanas todos os anos, segundo a Comissão Europeia. O aumento das AMR significa custos acrescidos não só para os sistemas de saúde, mas também para as empresas e serviços, que diminuem a produtividade.
- ⅙ dos europeus não sabe que o uso incorreto dos antibióticos os torna menos eficientes
- ⅓ dos europeus não sabe que os antibióticos têm efeitos secundários
- ½ dos europeus não sabe que os antibióticos não funcionam contra constipações e gripe
Desde a introdução da penicilina, nos anos 40, os antibióticos tornaram-se essenciais em vários tipos de tratamentos nos humanos e animais. São usados não apenas nos casos das doenças causadas pelas bactérias diretamente, mas também nos doentes que têm o sistema imunitário debilitado, como os seropositivos ou pessoas sujeitas a quimioterapia, e nos pacientes que se preparam para uma intervenção cirúrgica.
“Os antibióticos apoiam quase tudo na vida moderna”, lembrou a jornalista de saúde pública Mary McKenna, numa Ted Talk (um formato de conferência). “Se perdermos os antibióticos, também perderemos toda a proteção para pessoas com o sistema imunitário debilitado – doentes com cancro, com sida, recetores de transplantes, bebés prematuros -, depois todos os transplantes que introduzam objetos estranhos no organismo – diálise, substitutos de articulações [como os atletas]”, acrescenta. “Perdíamos a confiança na vida do dia-a-dia se soubéssemos que a mais pequena lesão nos podia provocar a morte.”
A jornalista continua dizendo que, se a situação se mantiver, vai tornar-se impossível fazer cirurgias – não se opera o coração, não se faz biópsias, nem cesarianas –, e que teremos de temer as infeções como outrora, quando a inflamação da garganta podia levar a uma falência no coração, quando as infeções na pele levavam à amputação do membro, quando dar à luz, mesmo no hospital mais limpo, matava uma em cada 100 mulheres ou quando uma pneumonia matava três crianças em cada 10.
“Estimamos que entre 38,7% e 50,9% dos patogénicos que causam infeções depois das cirurgias e 26,8% dos patogénicos que causam infeções depois da quimioterapia são resistentes aos antibióticos profiláticos padrão nos Estados Unidos”, refere uma equipa de investigadores num artigo publicado na revista científica The Lancet Infectious Diseases.
O que é que aquilo que comemos tem a ver com tudo isto?
O uso de antibióticos não está restrito à saúde humana ou à saúde dos animais de companhia. Os antibióticos são, em muitos casos, utilizados em grandes quantidades na pecuária, na aquacultura ou na agricultura. O objetivo, nos animais, é que evite o aparecimento de infeções e que potencie o seu crescimento, na agricultura também se pretende evitar a infeção bacteriana dos alimentos, como os cereais.
Cientes de que para combater a AMR é necessário um esforço conjunto, a Federação de Veterinários da Europa e o Comité Permanente de Médicos Europeus assinaram esta segunda-feira – no início da Semana Mundial para a Sensibilização sobre o Antibiótico – um memorando de entendimento para cooperação entre as duas entidades. O objetivo é tratar a resistência antimicrobiana em medicina humana e medicina veterinária como um único problema – “One-health problem”.
#epruma message on #EAAD it's about responsible AB use – use them as little as possible & as much as necessary
— EPRUMA (@epruma1) November 18, 2015
É fácil de imaginar que os antibióticos usados na agricultura chegam facilmente ao solo e às águas, mas acontece o mesmo com os antibióticos que são dados aos homens e aos animais. 80 a 90% dos antibióticos ingeridos não são degradados no sistema digestivo e são expelidos do organismo de ainda intactos, refere a Direção-Geral de Saúde (DGS). Mais, as estações de tratamento de águas residuais não têm capacidade de eliminar os antibióticos das águas.
A presença de antibióticos nas águas e nos solos, onde existem inúmeras bactérias, potencia o aparecimento de bactérias resistentes a esses antibióticos que em algum momento podem não só infetar os humanos (e animais) como transmitir os genes resistentes a bactérias que de outra forma conviveriam de forma pacífica com o homem.
#epruma promotes #responsibleuse of ABs in animals: discover new brochure – https://t.co/hvWyD4tlXN pic.twitter.com/LmGcGvdGXw
— EPRUMA (@epruma1) November 18, 2015
A recomendação é que se reduza significativamente o uso de antibióticos na agropecuária, especialmente as classes de antibióticos que são importantes na medicina humana, para diminuir a probabilidade de se criarem resistências. Adicionalmente, o uso de antimicrobianos como promotores de crescimento nos animais está proibido, desde 2006, segundo as recomendações da Comissão Europeia. E o uso de enzimas, probióticos e agentes descontaminantes está sujeito a autorização especial, não só para a medicina veterinária como também na saúde humana.
Um dos alertas mais importantes em relação às bactérias resistentes em animais foi publicado em 2008 pela EFSA e apresentava os porcos como sendo um reservatório importante de uma nova estirpe de Staphylococcus aureus resistente à meticilina (MRSA, na sigla em inglês para “meticillin-resistant Staphylococcus aureus”).
Num artigo publicado esta semana na revista científica The Lancet Infectious Diseases os investigadores apresentavam um novo gene que permite às Escherichia coli, e provavelmente a outras bactérias da famíli Enterobacteriaceae, resistir às polimixinas – um antibiótico de última linha. Esta resistência – a primeira deste tipo – foi encontrada sobretudo em porcos, num trabalho de investigação conduzido na China.
Que bactérias resistentes estão entre as que requerem mais atenção?
Os dados mais recentes do Centro Europeu para a Prevenção e Controlo de Doenças (ECDC, na sigla em inglês), que reúne os dados recolhidos pelos Estados-membros da União Europeia entre 2011 e 2014, mostra que a resistência antimicrobiana continua a aumentar. No relatório as principais preocupações são a resistência a antibióticos de terceira geração e até de última linha, como os carbapenemes, de estirpes resistentes de Escherichia coli e Klebsiella pneumoniae.
Esta é uma tendência que já tinha sido apontada no relatório de 2014, que apresentava os dados recolhidos entre 2008 e 2012. As bactérias resistentes aos carbapenemes (CPE, na sigla em inglês para “Carbapenemase-producing Enterobacteriaceae”), como E. coli e K. pneumoniae, conseguem produzir enzimas carbapenemase capazes de quebrar as moléculas dos antibióticos (não só as dos carbapenemes, mas também os de primeira, segunda e terceira geração). Adicionalmente, existem várias classes destas enzimas que estão restritas em termos geográficos, a não ser que uma pessoa seja tratada fora do país de origem e leve a estirpe resistente de volta a casa.
Principais grupos de antibióticos são:
- penicilinas, inibidores de betalactamase, cefalosporinas;
- monobactâmicos;
- carbapenemes;
- glicopeptídeos,
- macrólidos e lincosaminas;
- tetraciclinas;
- quinolonas e fluoroquinolonas;
- aminoglicosídeos;
- outros antibacterianos (exemplo: sulfonamidas, cloranfenicol, rifamicinas, linezolide, metronidazol, fosfomicina)
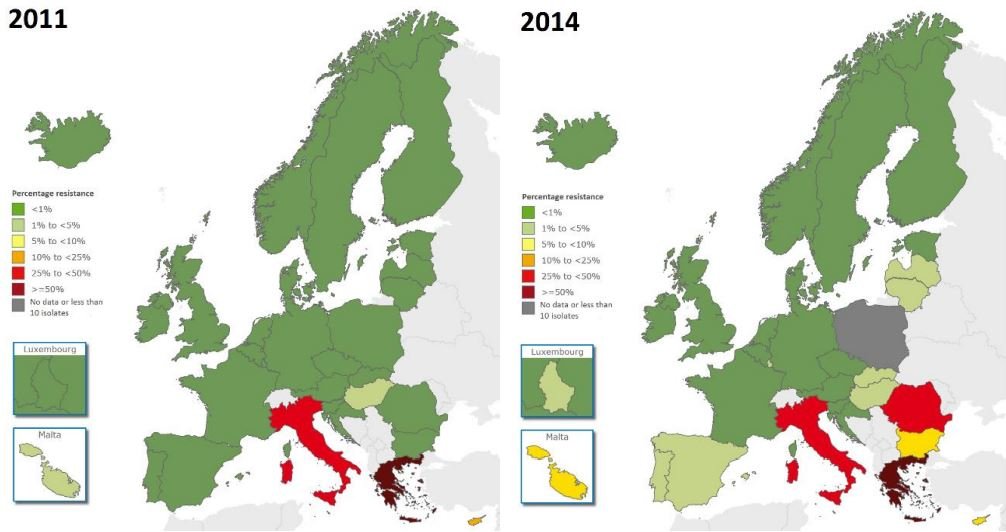
A Escherichia coli é uma das bactérias presentes no intestino, mas o crescimento descontrolado pode levar a infeções urinárias ou à contaminação da corrente sanguínea. Esta é também uma das bactérias mais comuns nos casos de infeção, uma situação particularmente grave, considerando que a maioria das estirpes é resistente a pelo menos um antibiótico. A resistência da bactéria a antibióticos de terceira geração também cresceu e até à combinação de vários destes antibióticos também subiu.
Resistência da Escherichia coli a antibióticos de terceira geração, neste caso cefalosporinas (dados de 2012) – EARS-Net/ECDC
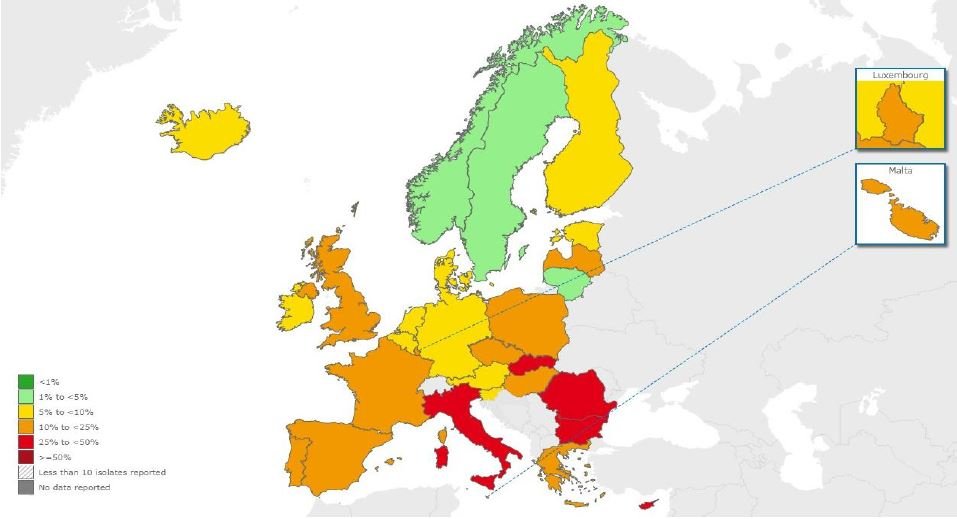
A bactéria Staphylococcus aureus existe na nossa pele e mucosas (como no nariz) e podemos conviver com ela sem nos causar problemas. Mas as infeções com S. aureus são também as mais comuns entre as infeções hospitalares (infeções contraídas no hospital), porque os equipamentos ficam facilmente contaminados – as mobílias hospitalares, as coberturas, os tubos de alimentação ou até os teclados dos computadores.
A distribuição da bactéria resistente MRSA em 2012 e Portugal entre os países com maior incidência – EARS-Net/ECDC
O problema é ainda maior quando se trata das estirpes resistentes, como a MRSA (na sigla em inglês para “meticillin-resistant Staphylococcus aureus“). Segundo o relatório de 2014 do ECDC, a incidência de MRSA está estabilizada ou até a diminuir em alguns países da Europa, mas sete dos 29 países que reportaram os dados – incluindo Portugal – continuam a ter uma taxa de MRSA superior a 25% comparada com as estirpes não resistentes da bactéria.
Estão particularmente em risco de ter uma infeção deste tipo os pacientes que vão ser submetidos a procedimentos invasivos, que já foram tratadas com antibióticos, que tiveram muito tempo no hospital ou nos cuidados intensivos ou pessoas que estiveram em contacto com pessoas portadoras da estirpe resistente.
O que é o problema crescente da Klebsiella pneumoniae?
A Klebsiella pneumoniae é uma causa comum de infeções urinárias, respiratórias e no sangue e consegue disseminar-se rapidamente em contexto hospitalar, refere o ECDC. Foi esta bactéria que causou o problema no Centro Hospitalar de Vila Nova de Gaia/Espinho.
Esta bactéria é motivo de preocupação adicional por parte do ECDC porque a maior parte dos casos reportados pelos Estados-membros era resistente a pelo menos um dos antibióticos e a resistência a combinações de vários antibióticos também era comum. A resistência crescente a vários antibióticos, incluindo os de terceira geração, diminui as opções terapêuticas para tratar esta bactéria.
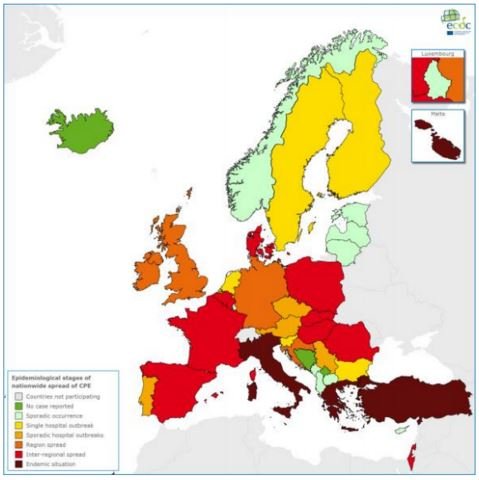
Distribuição das bactérias da família Enterobactericeae que produzem carbapenemase que as tornam resistentes a antibióticos (dados de 2015) – EARS-Net/ECDC
Para os casos em que há resistência à terapia combinada de vários antibióticos, o uso dos de última linha, como os carbapenemes podia ser uma opção. O problema é que a resistência a este tipo de antibiótico também está a aumentar, em especial na Europa do sul e leste. Usar outras combinações de antibióticos ou voltar a antibióticos antigos, como as polimixinas, pode ser uma opção, mas não pode ser generalizada, porque também já foi reportada a resistência desta bactéria a este antibiótico.
Neste momento, o ECDC recomenda uma vigilância mais apertada para identificar os potenciais portadores da estirpe resistente, como as pessoas que venham de outros países – porque as bactérias não conhecem fronteiras. Os doentes com alto risco de contraírem a infeção devem fazer imediatamente o despiste e se possível ser isolados. E todas as pessoas que contactaram com o doente devem ser identificadas e testadas.
For #EAAD ECDC releases results of European survey on spread of carbapenemase-producing Enterobacteriaceae in Europe https://t.co/031UbaGHjE
— ECDC (@ECDC_EU) November 16, 2015
Qual é o ponto de situação em Portugal?
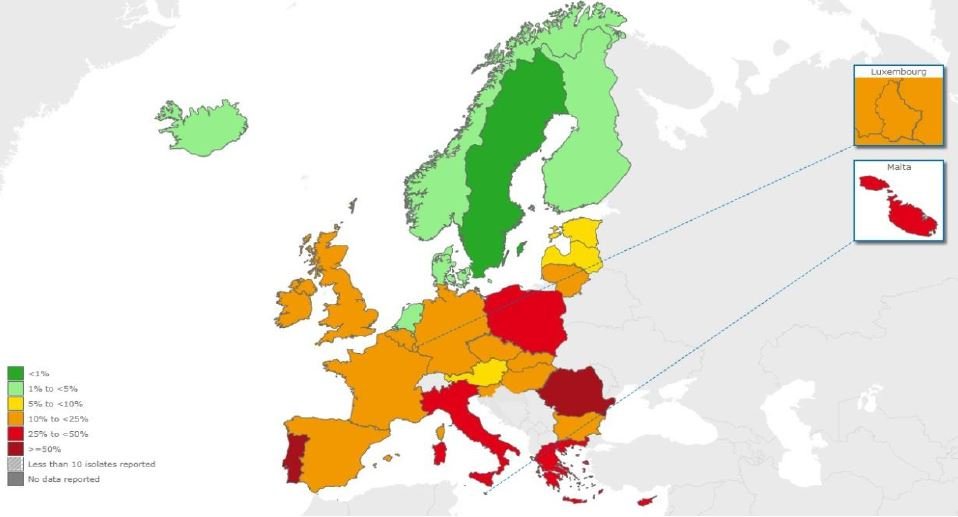
Portugal não se apresenta numa boa situação em relação as resistências antimicrobianas. O país apresenta um dos níveis mais elevados da Europa em termos de resistência do Staphylococcus aureus à meticilina (MRSA), refere a DGS. Desde 2003, a percentagem de MRSA tem crescido nas amostras da bactéria S. aureus – 45,5% em 2003 e 53,8% em 2012, com uma pequena descida em 2009 (49,1%). Os dados preliminares de 2013 apontam para 47%, representando uma descida importante na presença da bactéria resistente.
Além da S. aureus, a resistência de Acinetobacter spp. também faz Portugal aparecer entre os países com piores resultados. A bactéria apresenta uma elevada resistência a qualquer um dos seguintes antibióticos: fluoroquinolonas (77,4%), aminoglicosídeos (65,1%) e carbapenemes (79,2%), e ainda ao uso combinado destes antibióticos (64,3%).
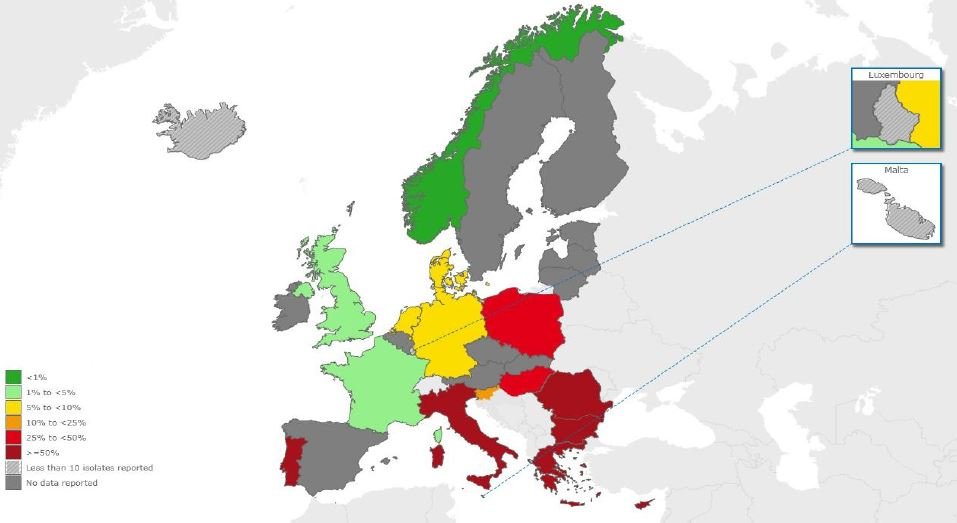
Portugal está entre os países onde há mais casos de Acinetobacter spp. resistentes a carbapenemes – EARS-Net/ECDC
A resistência de Klebsiella pneumoniae às cefalosporinas de terceira geração é um problema crescente na Europa em geral, mas também em Portugal. Em seis anos a percentagem de bactérias resistentes nas amostras subiu de 20,8% (2006) para 38,7% (2012). A percentagem de bactérias multirresistentes, ou seja, que apresentam resistência à utilização combinada de cefalosporinas de terceira, geração, fluoroquinolonas e aminoglicosídeos aumentou de 8,4%, em 2006, para 25,1% em 2012.
Com uma percentagem menor de bactérias resistentes, mas ainda assim preocupante, está a Escherichia coli, que, em Portugal, cresceu de 18% para 30%, entre 2001 e 2012. K. pneumoniae, E. coli, as estirpes do género Proteus e Enterobacter pertencem todas à mesma família – Enterobacteriaceae – e mostram uma resistência crescente a carbapenemes. Também com resistência crescente a este tipo de antibióticos aparece a Pseudomonas aeruginosa – a taxa de resistência aumentou de 16%, em 2009, para 20%, em 2012.
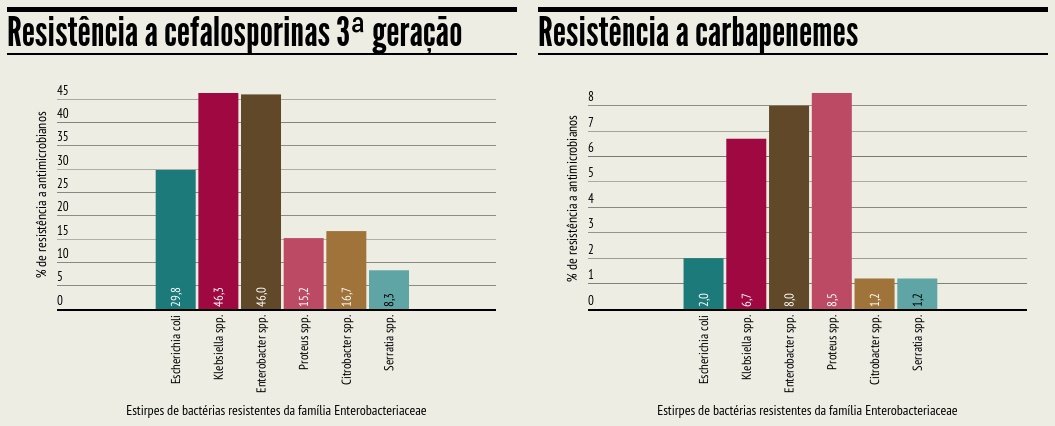
Dentro da família das Enterobacteriaceae, o género Enterobacter é o que apresenta maior taxa de resistência em Portugal (dados de 2012) – DGS/ECDC
Parte dos resultados sobre a resistência aos antibióticos parece ser suportado pelo consumo de antibióticos no país, sobretudo fora do contexto hospitalar. Entre 2008 e 2012, Portugal não mudou significativamente o consumo de antibióticos fora do contexto hospitalar, uma média de 22,8 doses diárias por cada mil habitantes nesse período – 22,7 em 2012.
Apesar de estar apenas um pouco acima da média da União Europeia (21,5) e muito longe da Grécia (31,9), Portugal está entre os países com maior uso de antibióticos fora dos hospitais. O país com uso menor é a Holanda, com 11,3 doses diárias por mil habitantes. Em relação ao uso de antibióticos em contexto hospitalar em Portugal, o ECDC só conseguiu dados dos hospitais públicos. Mas os dados gerais do ECDC indicam que metade da utilização de antibióticos nos hospitais é inadequada.
https://twitter.com/kgrindrod/status/665553364348981248
Um dos casos que merece atenção acrescida em Portugal é a gonorreia – doença sexualmente transmissível causada pela bactéria Neisseria gonorrhoeae. “Esta é uma das bactérias que tem mais facilidade em se tornar resistente aos antibióticos”, disse Filomena Pereira, médica microbiologista da Unidade de Clínica das Doenças Tropicais do Instituto de Higiene e Medicina Tropical. Por este motivo, o tratamento usado para combater a doença mudou. “A recomendação é que se usem dois antibióticos em simultâneo.”
O que é que os profissionais de saúde podem fazer?
Cabe aos profissionais de saúde fazerem uma boa prescrição dos antibióticos e informarem os doentes sobre a condição clínica e o bom uso destes medicamentos, mas, segundo os Centros de Controlo e Prevenção de Doenças norte-americanos (CDC, na sigla em inglês), 20 a 50% dos antimicrobianos prescritos a humanos são inadequados.
“Se um médico der ao doente opções de tratamento que o ajudem a aliviar os sintomas da doença pode ser uma forma de lidar com a satisfação dos pacientes. A maior parte das vezes, os doentes só procuram alívio e segurança”, disse Lauri Hicks, do gabinete de “Antibiotic Stewardship” dos Centros de Controlo e Prevenção de Doença norte-americanos (CDC).
Embora possa sentir pressão do doente para prescrever um antibiótico, o médico pode aliviar os sintomas das queixas típicas do inverno com outros medicamentos mais eficazes, como analgésicos para as dores, antipiréticos para a febre, expetorantes para descongestionar as vias respiratórias, anti-histamínicos para aliviar os sintomas das alergias. Mesmo no dentista, o uso de antibióticos deve ser restrito às excisões e não às inflamações.
“O que acontece muitas vezes é que quando se está a trabalhar sob pressão e como não há tempo para fazer uma história completa e observação mais minuciosa da criança, acaba por o doente levar um antibiótico por uma questão de precaução. É um erro recorrente”, disse Libério Ribeiro, Presidente da Sociedade Portuguesa de Alergologia Pediátrica, em relação às situações em que os pais exigem antibióticos para os filhos.
O médico deve conversar com o doente, explicar qual a doença, quais os sintomas esperados e durante quanto tempo se podem manifestar, como se deve tratar e porque não deve ser tratado de outra forma (com antibióticos, por exemplo). Adicionalmente, identificar os doentes portadores de bactérias resistentes, ajuda a prevenir a contaminação de outras pessoas, melhora o tratamento desse doente e reduz os custos do sistema de saúde, refere um relatório da Agência para a Proteção e Promoção de Saúde do Ontário.
Algumas recomendações:
- evitar o uso inapropriado ou excessivo de antibiótico enquanto medida terapêutica ou profilática;
- assegurar que os antibióticos são dados com a dosagem correta e com a duração ideal;
- reduzir o uso de antibióticos de largo espetro, especialmente os de terceira geração, e reservá-los para as situações em que são mesmo necessários;
- estabelecer programas de gestão da utilização de antibióticos (“antibiotic stewardship”) nas instituições.
De facto, a publicação da Norma de Profilaxia Antibiótica Cirúrgica, em dezembro de 2013, estabelece que cirurgias carecem da toma de antibióticos preventivamente, qual o melhor momento e a dose – nunca por mais de 24 horas. No mesmo ano, em julho, a Norma de Duração da Terapêutica Antibiótica define que, como regra geral, não se devem tomar antibióticos por mais de sete dias.
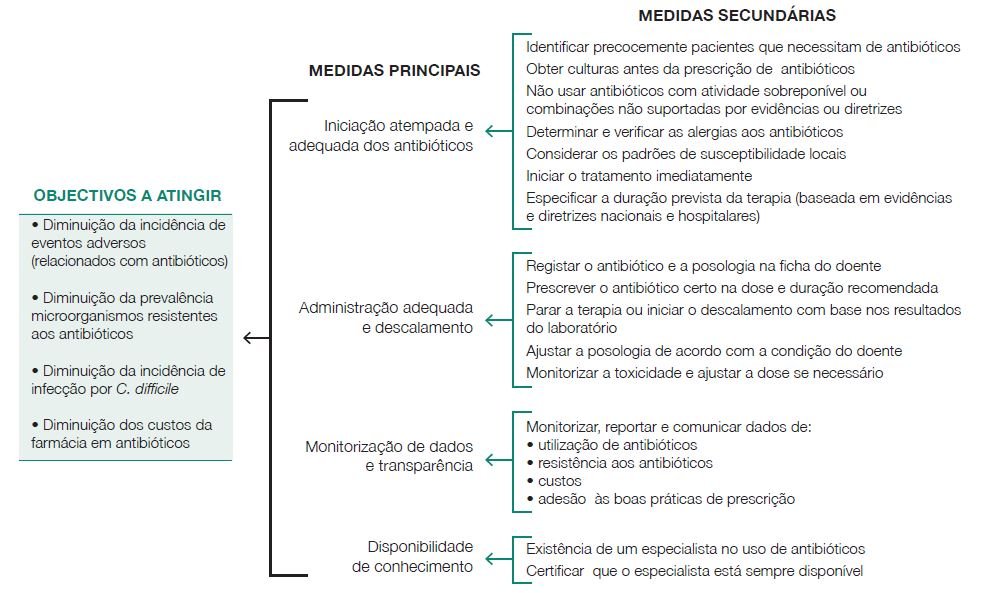
Exemplo de Diagrama de Objetivos, retirado do Guia prático para a implementação de Programas de Gestão de Utilização de Antibióticos publicado pelo IHMT/UNL – Simões et al. (2015) IHMT-UNL
A DGS recomenda a implementação de Programas de Gestão de Utilização de Antibióticos (ou “Antibiotic Stewardship”) para reduzir a prevalência da resistência aos antimicrobianos, diminuir os custos com os cuidados de saúde e ser mais bem-sucedido no tratamento dos doentes. Neste processo tem de estar envolvida uma equipa multidisciplinar, com médicos, enfermeiros, microbiólogos, farmacêuticos e gestores.
Estes programas preveem a criação de um plano de ação por parte da equipa, a monitorização das prescrições e dos padrões de resistência identificados, a avaliação constante da evolução do doente para adaptar a terapia caso seja necessário, a comunicação transparente de todas as situações identificadas e a educação de profissionais de saúde, doentes e público em geral.
Claro que para estes programas funcionarem é preciso que as administrações dos hospitais os apoiem, lembrou Lauri Hicks. “É preciso convencer a administração que, não só melhoramos a qualidade dos cuidados prestados aos doentes – melhoramos a recuperação dos doentes e reduzimos a mortalidade -, mas também reduzimos custos.” E estes são pontos-chave para os gestores hospitalares.
A indústria farmacêutica faz parte da solução ou do problema?
É imperativo que se desenvolvam novos antibióticos ou formas alternativas de tratamento, mas o investimento da indústria farmacêutica neste tipo de medicamentos tem sido cada vez menor. “Têm de ser encontradas soluções para os problemas relacionados com a vigilância global, esforços e investimento (público e privado) para investigação e desenvolvimento – que estão presentemente fragmentados e, por vezes, duplicados”, disse ao Observador a diretora dos assuntos europeus da Federação Europeia de Indústrias e Associações Farmacêuticas (EFPIA, na sigla em inglês), Elizabeth Kuiper.
Se houve uma altura em que era relativamente fácil encontrar novos antibióticos, agora este trabalho é cada vez mais moroso e dispendioso, com muitos becos sem saída até se chegar a um antibiótico seguro e eficaz. Depois do tempo e dinheiro investido, a venda de antibióticos é pouco rentável: a prescrição é cada vez mais restrita, os tratamentos não são prolongados e, se os microrganismos desenvolverem resistência, o medicamento pode ter de ser abandonado. Além disso, o mercado dos genéricos tem dominado o mercado dos antibióticos nos últimos anos.
“Claro que devemos procurar novos antibióticos, mas o que vimos no passado é que, se mantivermos o mesmo comportamento que temos tido até agora com os novos antibióticos, também se vão desenvolver resistências contra esses”, alertou Andrea Ammon, diretora do Centro Europeu de Controlo e Prevenção da Doença. “Precisamos de uma mudança de base na atitude.”
A instituição que Elizabeth Kuiper representa defende assim que devem ser os sistemas de saúde a financiar a investigação, porque são eles os principais beneficiários do produto e ao mesmo tempo o organismo responsável por controlar as infeções. A diretora dos assuntos europeus considera, no entanto, que os sistemas de saúde só devem pagar em caso de sucesso. E acrescenta que apoia a criação de um novo modelo de negócio para a indústria farmacêutica que não seja baseado nas vendas. “[Assim] as empresas já não se sentiam tentadas a vender tanto quanto pudessem.”
Enquanto a procura e fabrico de antibióticos não se mostrar um negócio rentável para as indústrias farmacêuticas, estas continuarão a investir nos medicamentos para as doenças crónicas. As restrições são ainda maiores (e o negócio menos rentável) no que diz respeito à medicina veterinária. Mas Elizabeth Kuiper concorda que terá de haver um espírito de cooperação entre os vários agentes envolvidos no processo para combater em problema em conjunto. Além disso, a EFPIA apoia os Programas de Gestão de Utilização de Antibióticos, considerando que a indústria tem de fazer parte da solução.
.@kuiper_em of @EFPIA on need for #OneHealth in #AMR. Approach to animal health must not undermine ability to treat infections in humans
— Innovative Health Initiative (@IHIEurope) November 17, 2015
Os 12 pontos do plano de ação para combater a resistência antimicrobiana:
- Reforçar a promoção da utilização adequada dos agentes antimicrobianos em todos os Estados-Membros;
- Reforçar o quadro regulamentar no domínio dos medicamentos veterinários e dos alimentos medicamentosos para animais;
- Introduzir recomendações para a utilização prudente na medicina veterinária, incluindo relatórios de acompanhamento;
- Reforçar a prevenção e o controlo das infeções em ambientes de prestação de cuidados de saúde;
- Introduzir um instrumento jurídico na nova legislação em matéria de saúde animal, a fim de melhorar a prevenção e o controlo das infeções nos animais;
- Promover, seguindo uma abordagem por etapas, esforços de investigação e de desenvolvimento de uma forma colaborativa sem precedentes para proporcionar aos doentes novos antibióticos;
- Promover esforços para analisar a necessidade de novos antibióticos na medicina veterinária;
- Desenvolver e/ou reforçar os compromissos multilaterais e bilaterais para a prevenção e o controlo da RAM em todos os setores;
- Reforçar os sistemas de vigilância da RAM e o consumo de agentes antimicrobianos na medicina humana;
- Reforçar os sistemas de vigilância da RAM e o consumo de agentes antimicrobianos na medicina animal;
- Reforçar e coordenar os esforços de investigação;
- Inquérito e análise comparativa da eficácia.
Que contributos pode dar a comunidade científica?
Em duas décadas, desde 1940 até 1962 os cientistas descobriram mais de 20 classes de antibióticos. Mas já lá vão cinco décadas e só foram descobertas mais duas classes novas de antibióticos. Parte do problema é a dificuldade crescente em encontrar novos antibióticos, a outra é a escassez de financiamento.
Mas nem tudo depende do financiamento, disse ao Observador Mats Ulfendahl, presidente do conselho de administração do programa conjunto para combater a AMR (JPIAMR, na sigla em inglês para Joint Programming Initiative on Antimicrobial Resistance). “Existe uma crença de que investir mais dinheiro vai resolver o problema. Certamente que vai ajudar, mas temos de ter ideias. E é isso que queremos fazer com este programa conjunto – financiar as melhores ideias”, acrescentou. “Precisamos de mais financiamento, mas precisamos de o fazer de uma forma mais estratégica, de uma forma mais coordenada.”
Why a Joint Programming Initiative on #AMR ? #AntibioticResistance #EAAD https://t.co/kQ1nn8FfVI pic.twitter.com/vIFdDaZq27
— JPIAMR (@JPIAMR) November 18, 2015
Para Mats Ulfendahl a chave está em encontrar ideias que fujam ao convencional, que saiam da caixa. Muitas delas ficarão pelo caminho, mas outras hão de vingar. Isto ajudará a contrariar a tendência de colocar dinheiro onde já existe dinheiro, ou seja, nas áreas que são mais financiadas. Normalmente, diagnóstico do doente, ambiente envolvente e transmissão entre animais e pessoas, recebem pouco financiamento. E no campo do diagnóstico é importante encontrar mecanismos mais rápidos e baratos, especialmente para poder usar nos países em desenvolvimento.
“Um dos desafios que enfrentamos é que os testes para bactérias não são muito bons a detetar bactérias”, referiu Lauri Hicks, coordenadora do programa de sensibilização para AMR dos Centros de Controlo e Prevenção de Doença norte-americanos – “Get Smart: Know When Antibiotics Work”. “Essa é uma área onde precisamos de desenvolvimento: criar novos testes que nos ajudem a identificar o que estamos a tentar tratar.” Outra área é perceber se uma bactéria que se mostre resistente em laboratório, também o é dentro do corpo humano.
O programa JPIAMR pretende juntar vários grupos de investigação de vários países, para que cada um possa contribuir com aquilo que sabe fazer melhor e aprender com os restantes membros. Desta forma potencia-se o surgimento de novas ideias, ao mesmo tempo que se evita que existam trabalhos de investigação duplicados entre duas equipas que podem trabalhar juntas.
Depois de ter financiamento, e caso se chegue ao antibiótico, é preciso ter atenção à monitorização das terapias, para prevenir e detetar o aparecimento de bactérias resistentes. A higiene e a educação/formação dos profissionais de saúde, dos gestores e do público em geral também tem um papel importante.
Dos novos antibióticos, às novas abordagens, e voltando também aos antibióticos antigos para os modificar, podem surgir várias soluções para combater as infeções bacterianas, especialmente as resistentes. Sejam moléculas que amarram as bactérias e as impedem de atuar ou que bloqueiam os compostos libertados pelas células, seja a capacidade de interferir na transferência de material genético entre duas bactérias.
@AcumenPA @EU_Commission will co-fund a research call of the JPIAMR that will be issued in early 2016 https://t.co/vUVEw2RiXH #EAAD
— EU One Health (@EU_Health) November 18, 2015
Uma equipa de investigadores liderada por Kim Lewis, do Centro de Descobertas Antimicrobianas da Northeastern University, em Massachusetts (Estados Unidos), confirmou que a fonte de antibióticos com base em microrganismos do solo se esgotou nos anos 1960 pela dificuldade em cultivar as restantes bactérias em laboratório. Mas com isso ficaram 99% das espécies existentes no solo por estudar. Ora, é do estudo das bactérias e da interação com outros microrganismos que podem surgir novos antibióticos e a equipa norte-americana conseguiu arranjar maneira de conseguir manter as bactérias ativas no laboratório.
Além do solo, existem outros locais onde podem ser encontradas bactérias com potencial antimicrobiano – ou seja, que produzem moléculas que controlam o crescimento de outras bactérias: nas grutas dos Açores, no estômago das abelhas ou na vagina. E também se pode tentar impedir as bactérias de desempenharem funções normais, como quando tentam formar biofilmes ou se tentam multiplicar.
Como formas de investigação alternativa podem surgir, por exemplo, vírus capazes de atacar seletivamente bactérias, como a Escherichia coli, e torná-las mais suscetíveis aos antibióticos. A ideia é usá-los para esterilizar materiais hospitalares, para a limpeza de superfícies ou até no sabão de mãos dos cirurgiões, conforme foi publicado na revista científica Proceedings of the National Academy of Sciences of the United States of America.