“Não conseguimos vencer a guerra contra o cancro, mas estamos a conseguir vencer algumas batalhas”, diz o oncologista Paulo Cortes. E essas batalhas vencem-se quando se reduz o tempo de tratamento com as mesmas vantagens, mas com menos efeitos secundários, quando se desenvolvem novos tratamentos ou quando se aposta numa medicina personalizada (em que o tratamento é específico do doente). E todos os anos — para não dizer todos os meses — há novidades sobre novas armas e estratégias para usar nestas batalhas.
“A ciência está a evoluir no sentido da personalização dos tratamentos”, diz Gabriela Sousa, médica do Serviço de Oncologia Médica do Instituto Português de Oncologia de Coimbra. Porque não existe — e provavelmente nunca existirá — uma cura universal para o cancro. Não só o cancro do pulmão é diferente do cancro da mama e diferente do melanoma, como cada cancro do pulmão é diferente de pessoa para pessoa. “São doenças diferentes, em pessoas diferentes, com imunidades diferentes”, diz ao Observador Paulo Cortes, presidente da Sociedade Portuguesa de Oncologia.
Os congressos médicos da especialidade são um bom local de partilha de todos estas descobertas, dos resultados dos ensaios clínicos, da confirmação daquilo que já se sabia ou da apresentação de resultados completamente inesperados. Mas estes congressos falam numa linguagem própria: a linguagem dos médicos e investigadores. O que é que isto significa para os doentes e para as famílias?
O Observador falou com três oncologistas portugueses que estiveram na reunião anual da Associação Americana de Oncologia Clínica — 2018 ASCO Annual Meeting —, que reuniu mais de 30 mil participantes, para perceber o que de mais importante se discutiu nesta reunião e que impacto pode ter na prática clínica.
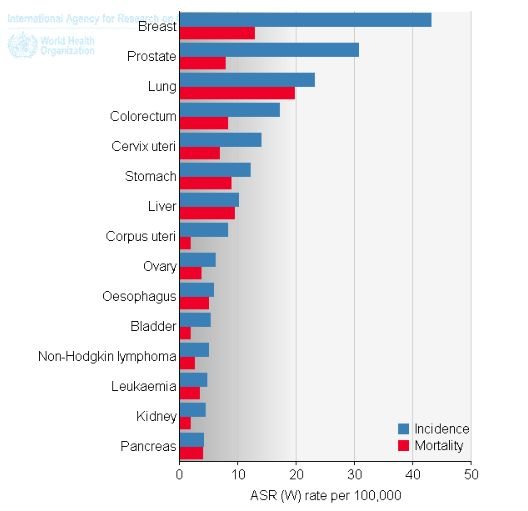
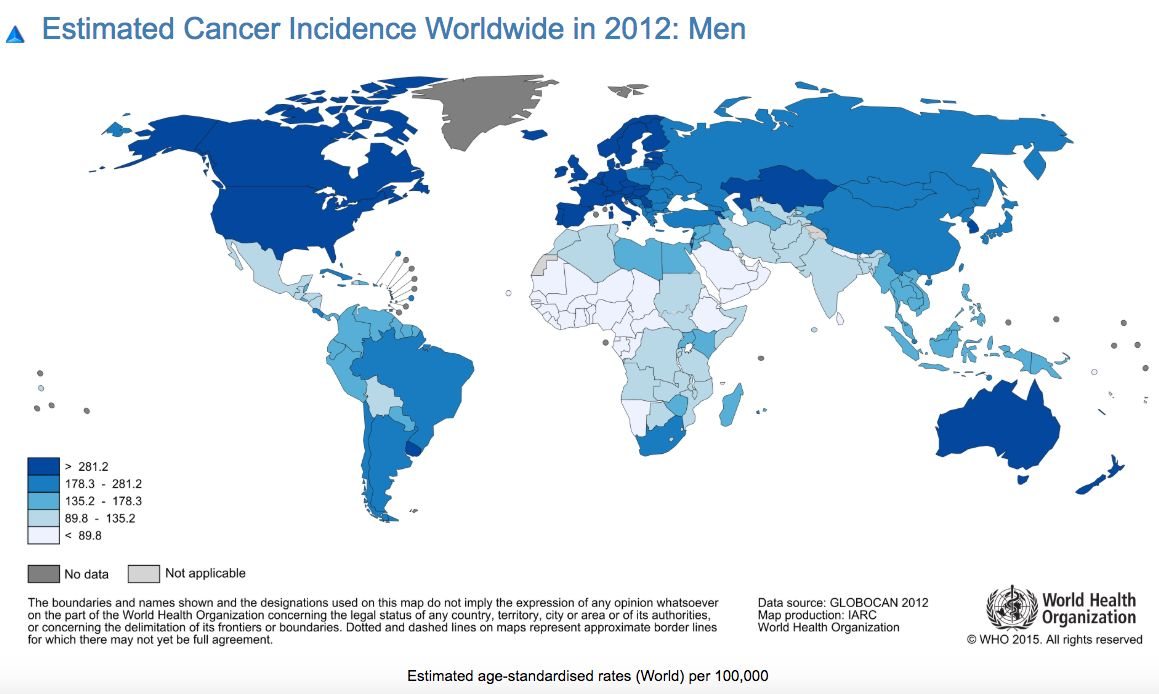
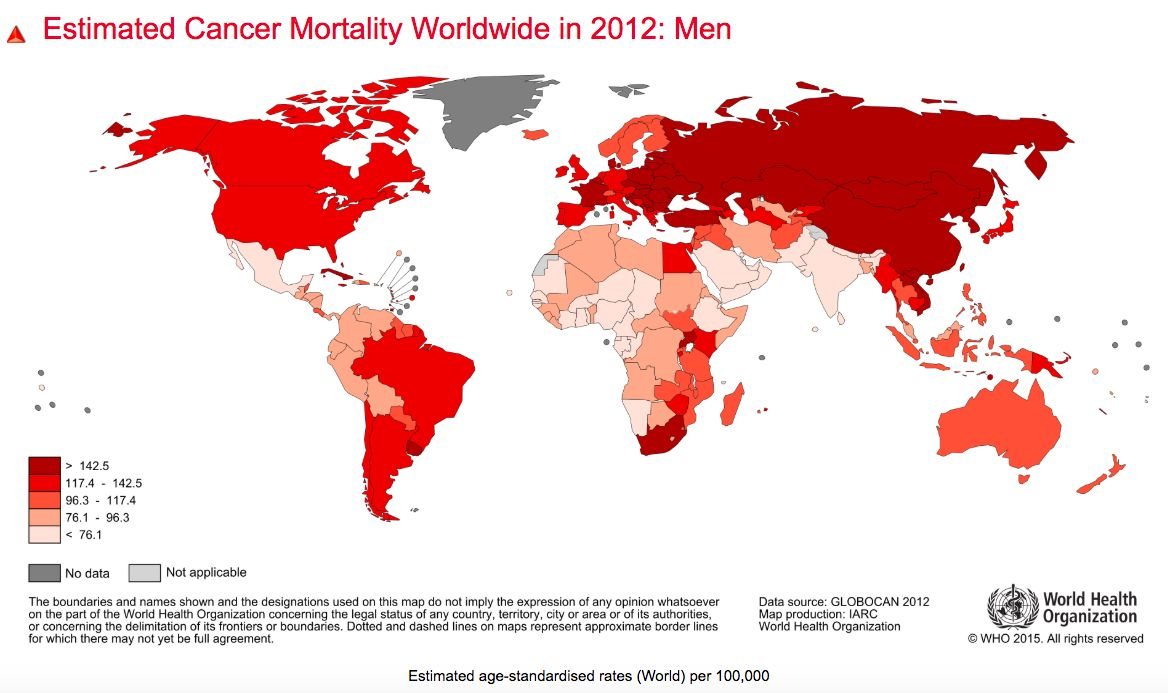
Estimativa da incidência de cancro e mortalidade causada pela doença. O cancro da mama e da próstata têm incidências altas, mas têm taxas de cura na ordem dos 70%. Apenas 40% dos cancros são preveníveis, mas deixar de fumar é a principal causa de cancro que se pode prevenir — WHO
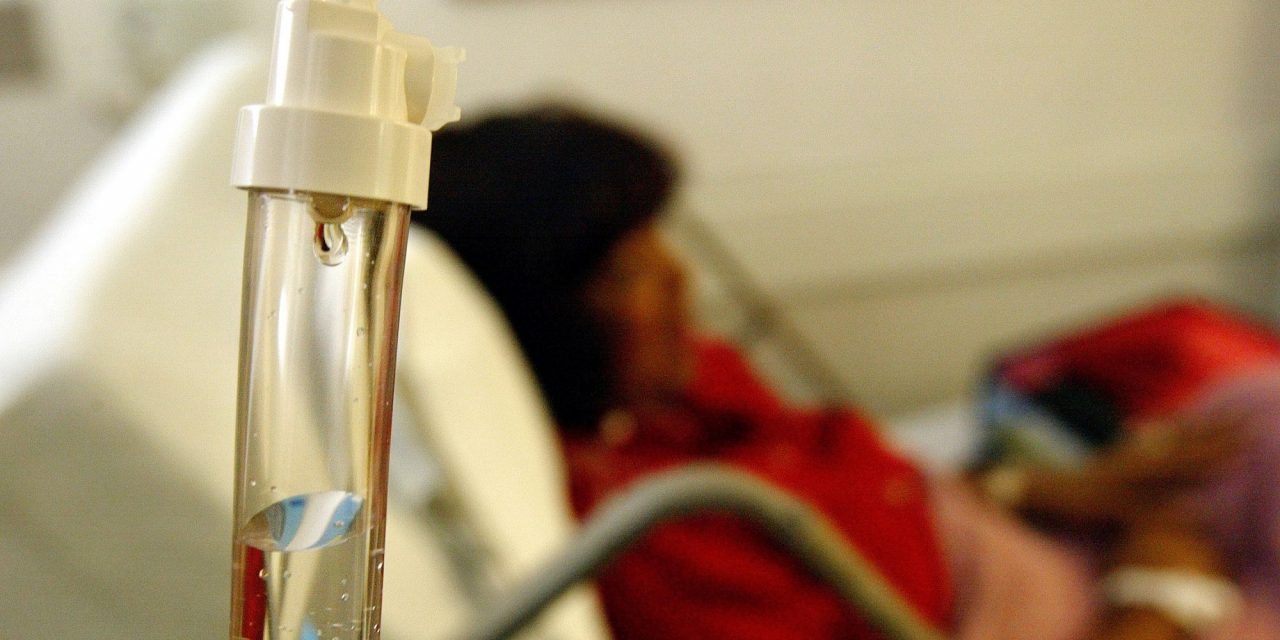
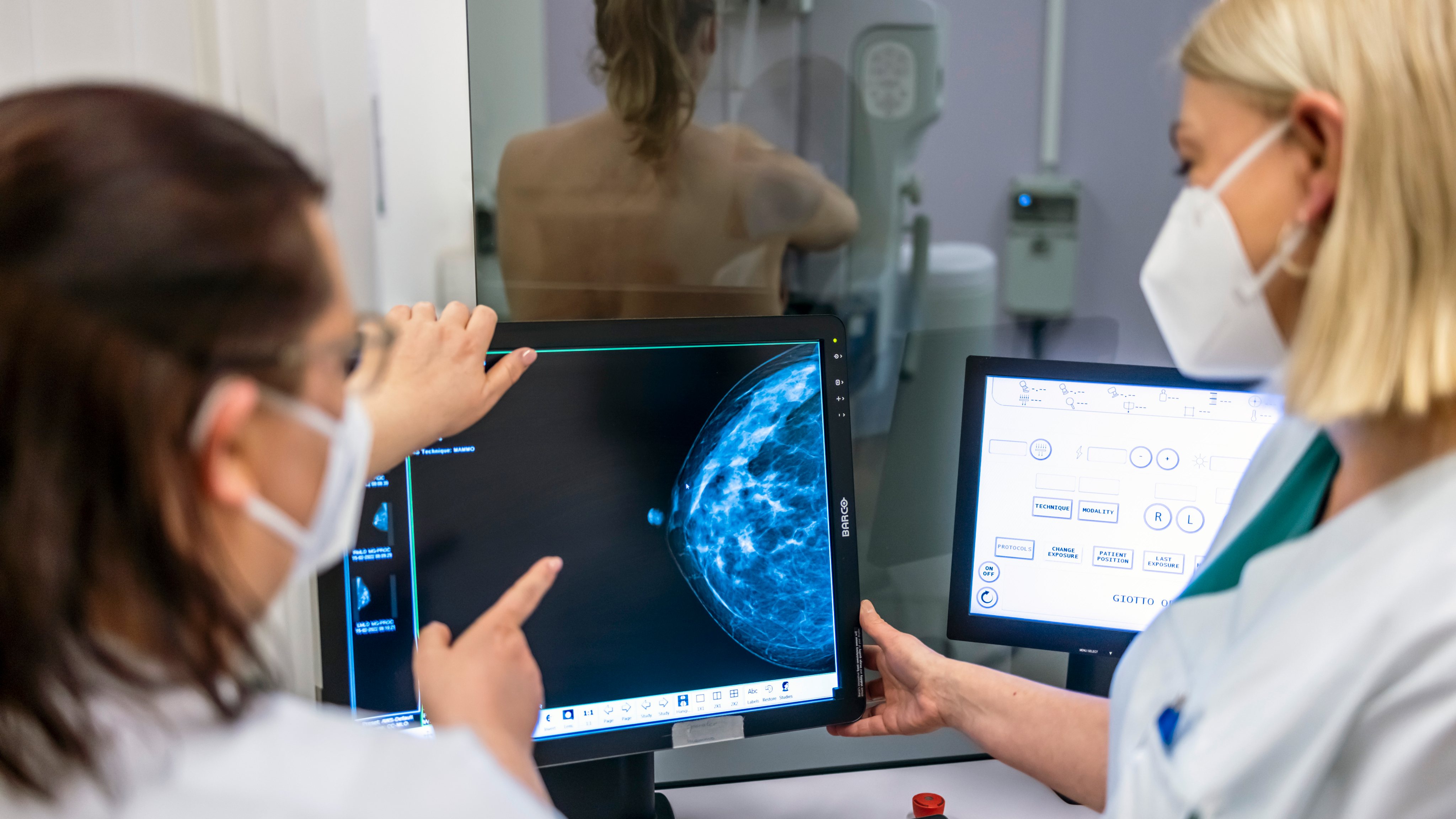
Como evitar a quimioterapia nas doentes com cancro da mama?
Ouvirmos dizer que a quimioterapia pode ser evitada em 70% das mulheres com cancro da mama são boas notícias, mas devem ser explicadas, porque não se referem a todos os tipos de cancro, nem as medidas vão ser aplicadas em toda a parte. É verdade que o estudo que chegou a estas conclusões foi feito com o tipo de cancro da mama mais frequente, ainda assim refere-se apenas a um tipo de cancro da mama: precoce, hormono-dependente, sem nódulos axilares e HER2-negativo.
A grande vantagem deste trabalho em relação a estudos anteriores, explica Paulo Cortes, é que este se trata de um estudo prospetivo, e não retrospetivo, ou seja, um estudo controlado que acompanha os doentes ao longo do tempo, e não um estudo baseado em dados do passado. “A aplicabilidade prática é imediata”, garante o médico.
Maioria das mulheres com cancro da mama poderá evitar quimioterapia
Os resultados foram baseados num teste genómico ao cancro da mama — Oncotype DX — que identificou 21 genes e vai beneficiar sobretudo quem tem acesso a este tipo de testes. “Nos Estados Unidos este tipo de teste genómico é pedido a todas as mulheres com cancro da mama hormono-dependente”, disse Fátima Cardoso, diretora da Unidade da Mama do Centro de Cancro Champalimaud. “Mas na Europa só se pede um teste genómico quando há dúvidas se a pessoa precisa de fazer quimioterapia.” A investigadora explica porquê: nos Estados Unidos, as seguradoras comparticipam estes testes, mas na Europa não. Cada teste genómico Oncotype DX custa 3.600 euros por doente, lembra Gabriela Sousa.
“Em Portugal, e em muitos países da Europa, os testes não são reembolsados nem pelas seguradoras, nem pela maioria dos sistemas de saúde.” Mas deviam, na opinião da médica. A esperança é que estes resultados sirvam de pressão para que passe a haver comparticipação. Paulo Cortes reforça que agora “temos dados de evidência científica de qualidade”, que se traduzem em “poupanças de recursos”.
Para Fátima Cardoso, os resultados são particularmente importantes para quem usa Oncotype DX e não sabe o que fazer com os casos de risco médio de recidiva (o risco de o cancro voltar a aparecer). Mas na Europa “não vai mudar o que se faz na prática”, afirma a médica, responsável pelas recomendações europeias para o cancro da mama (precoce e avançado).
Para decidir se um doente precisa de fazer quimioterapia para evitar recidivas avaliam-se as características do tumor — o tipo de tumor, grau de diferenciação das células, resposta a outros tratamentos — e o doente (como a idade e o estado de saúde geral). Se o risco é baixo, a terapia hormonal pode ser suficiente. Quando o risco é alto, a quimioterapia é fortemente aconselhada. Quando o risco é médio, podem surgir algumas dúvidas sobre que tratamento fazer, dúvidas essas que os testes genéticos podem ajudar a resolver.
“Já estávamos à espera do TailorX [Trial Assigning Individualised Options for Treatment] há muito tempo”, disse Fátima Cardoso, sobre o estudo agora apresentado. Este trabalho veio reforçar os resultados que a equipa da investigadora já tinha publicado em 2016 na revista The New England Journal of Medicine. Na altura, a equipa validou o teste Mammaprint com ensaios clínicos e verificou que 46% das mulheres, com cancro da mama em estádio inicial, que são classificadas como doentes de alto risco pelos métodos tradicionais poderiam evitar fazer quimioterapia.
As vantagens de evitar quimioterapia são claras, para o doente e para a sociedade. Por um lado, o doente evita todos os efeitos secundários da quimioterapia, como cansaço, náuseas, vómitos, queda de cabelo e, mais tarde, o risco de problemas cardíacos e outros tumores. Por outro, evitam-se os custos indiretos, como as faltas do doente ao trabalho ou os profissionais de saúde que deixam de estar alocados a esse tratamento.
Os testes genéticos e genómicos podem ajudar a escolher os melhores tratamentos?
Teste genético vs genómico
↓ Mostrar
↑ Esconder
Um teste genómico pretende analisar os genes do tumor, enquanto o teste genético se refere à análise dos genes da pessoa (doente ou não).
Paulo Cortes considera que a análise dos genes das células tumorais e dos doentes, e a interação com o microbioma, “tem tido um grande desenvolvimento e tem-se mostrado muito promissora”. Estas análises identificam alterações genéticas que podem, potencialmente, ser alvos terapêuticos para os medicamentos. É preciso é que esses fármacos estejam disponíveis. E é isso que faz Fátima Cardoso olhar de uma forma mais cautelosa para a possibilidade de estes testes ajudarem a escolher os tratamentos. “Ainda não existem medicamentos para todas as alterações que possam ser identificadas pelos testes genéticos ou genómicos.”
O presidente da SPO concorda que os testes genéticos não são solução para tudo, mas estes testes podem ajudar a selecionar que doentes podem beneficiar da imunoterapia e que tipo de resposta podem ter, por exemplo. “É uma revolução a começar. Estamos a dar os primeiros passos e precisa de ser integrada com calma, mas é irreversível.”
▲ Identificar os genes de uma pessoa tornou-se relativamente fácil. Saber o que fazer com os resultados nem tanto — chemicalbilly/Getty Images/iStockphoto
chemicalbilly/Getty Images/iStockphoto
Por enquanto, as recomendações europeias e norte-americanas dizem que este tipo de testes não deve ser usado, só nos ensaios clínicos. O problema é que há muitos testes genéticos disponíveis sem controlo nem regulamentação, alerta a Fátima Cardoso. E as pessoas chegam à consulta com o resultado dos testes à espera de uma solução. “Primeiro, é preciso perceber, entre todas as alterações do tumor, quais são realmente importantes, quais as que potenciam a malignidade do tumor. Em seguida é necessário desenvolver medicamentos que consigam chegar a esses alvos”, refere a investigadora para reforçar o longo percurso que ainda é preciso fazer.
Como melhorar a monitorização dos tratamentos?
Ainda sobre os testes genéticos, Gabriela Sousa não vê vantagens em generalizar este tipo de testes genéticos. A oncologista prefere falar de outra possibilidade: as biópsias líquidas, que analisam os nossos fluídos corporais (sangue, urina ou ar expirado) à procura de proteínas tumorais que possam ajudar a detetar a doença antes de esta se manifestar. “Ainda estamos longe da prática clínica, porque envolve tecnologia muito cara”, diz. Em estudo está, por exemplo, a possibilidade de usar biópsias líquidas para monitorizar a evolução dos tratamentos.
Teste sanguíneo capaz de detetar cancro pode vir a ser uma realidade
A especialista em tumores urológicos (rim, próstata, bexiga, testículos) dá como exemplo o carcinoma da próstata resistente à castração. Existem seis fármacos aprovados para o tratamento destes doentes, mas nem todos os tratamentos são igualmente eficazes com todos os doentes. “A biópsia líquida permite-nos perceber quais é que podemos eliminar à partida.”
Mas as biópsias líquidas não são a única hipótese de monitorizar os tratamentos e também aqui podem haver melhorias. Durante o encontro, um grupo de investigadores mostrou que um método de diagnóstico, que já existe em Portugal (PET PSMA), usado em doentes que foram sujeitos a cirurgia ou quimioterapia, era mais eficaz a detetar metástases e conseguia fazê-lo mais cedo. Isto permite que os doentes iniciem ou mudem de tratamento mais cedo também, explica Paulo Cortes.
A imunoterapia é solução para todos os problemas de cancro?
Sobre a imunoterapia, Fátima Cardoso apressa-se a dizer que “não é uma panaceia” e “não vai dar a cura para o cancro”. “É uma nova arma que estamos a aprender a usar, mas só funciona com alguns tipos de cancro.” Além disso, precisa de ser coadjuvada com radioterapia ou quimioterapia.
Paulo Cortes concorda que não é um tratamento universal, mas defende que a imunoterapia representa uma mudança de paradigma, porque é uma abordagem transversal a vários tumores, em vez de ser uma abordagem confinada a cada tipo de tumor. “Têm-se falado muito de imunoterapia e com justiça, porque tem feito uma enorme diferença para alguns tipos de tumores e tem tido boas respostas em tumores de fases avançadas”, diz o oncologista.
Os melhores resultados para a imunoterapia têm sido encontrados nos tumores que têm mais mutações genéticas, como o melanoma ou alguns subtipos de cancro do pulmão, nomeadamente cancro do pulmão de células não-pequenas. Neste encontro, não houve novidades em relação ao tratamento do melanoma, conta o especialista neste tipo de tumor, mas os estudos apresentados tornaram mais sólidos os conhecimentos existentes. Já no caso do cancro do pulmão, além dos trabalhos que consolidam os conhecimentos prévios, houve também novidades: os cancros do pulmão de células escamosas e de pequenas células podem beneficiar de tratamentos de imunoterapia. Por enquanto, é preciso esperar por mais estudos que confirmem estes resultados.
Medicamento contra cancro do pulmão com comparticipação aprovada
Em oposição, a imunoterapia não tem mostrado grandes resultados com o cancro da mama, lembra Fátima Cardoso. “Talvez com o cancro da mama triplo negativo [quando o cancro da mama não é hormono-dependente nem HER2-positivo] venha a ter um papel importante.” Este subtipo de cancro da mama tem, pelo menos, sete subgrupos identificados e ainda não existe tratamento específico para nenhum deles.
Em relação ao caso de Judy Perkins, uma norte-americana que foi sujeita a uma nova técnica de imunoterapia para tratar um cancro da mama metastático, Fátima Cardoso não vê razão para ter sido publicado na Nature Medicine. “A doente não está curada, está em remissão completa. A doença não é visível, mas não desapareceu”, lembra a médica. “Já tive doentes, a fazer só hormonoterapia, em remissão completa durante quatro ou cinco anos, mas, eventualmente, a doença regressa.” Deste caso, a investigadora retira aquilo que se pode aprender com as pessoas que tiveram resultados excecionais para ajudar a tratar os outros doentes.
Fátima Cardoso lembra que todos os anos 1,7 milhões de mulheres são diagnosticadas pela primeira vez com cancro da mama. A técnica usada é específica para cada pessoa, o que implica que demore muito tempo, custe muito dinheiro e que seja logisticamente difícil de aplicar. Para a investigadora, é muito difícil que se venha a tornar um tratamento corrente.
Judy Perkins era um caso incurável, a quem os médicos tinham previsto três meses de vida. São estes casos, os incuráveis pelos meios de tratamentos disponíveis, que são convidados a participar nos ensaios clínicos com tratamentos inovadores. Só se os medicamentos se mostrarem eficazes e seguros, pode o ensaio ser alargado a outros doentes. “Não podemos alterar o tratamento de um cancro potencialmente curável com um tratamento experimental”, justifica a médica.
Usar duas imunoterapias para vencer um cancro da mama difícil
Conseguimos aumentar a esperança de vida em doentes com cancro do pâncreas?
Nos encontros médicos, tanto podem ser anunciados tratamentos inovadores, como serem apresentados mais dados que confirmem estudos anteriores ou pequenas alterações que podem mudar as práticas clínicas. Um dos exemplos para este último caso foi referido por Paulo Cortes e diz respeito ao cancro do pâncreas, “um tumor muito difícil de tratar”.
Quando o cancro do pâncreas é identificado numa fase inicial — quando ainda está localizado no órgão e não tem metástases — é removido cirurgicamente. Por vezes, a cirurgia consegue remover o tumor na totalidade, mas nem sempre isso acontece. Às vezes, ficam algumas células para trás, que podem dar origem a um novo tumor. Um tratamento convencional de quimioterapia, com gemcitabine, depois da cirurgia aumenta o tempo de sobrevida dos doentes quando comparado com a cirurgia só por si. Mas agora há uma nova proposta.
Um ensaio clínico de fase III mostrou que se estes doentes fossem submetidos a um tratamento de quimioterapia normalmente usado com doentes metastáticos — Folfirinox — viviam em média mais 21,6 meses (contra 12,8 meses com o tratamento convencional) e ficavam livres de cancro mais nove meses do que quem fez o tratamento convencional, com gemcitabine. A desvantagem é que esta quimioterapia é mais agressiva e tem mais efeitos secundários que o tratamento convencional. Logo, não poderá ser usada com todos os doentes, esclarece Paulo Cortes.
“Provavelmente vamos passar a usar”, disse o médico, sobre o tratamento que já é feito em Portugal para doentes em estado avançado. “Mas temos de escolher os doentes que têm melhores condições para o fazer, porque é muito agressivo.”
Um dos problemas do cancro do pâncreas é que é difícil de detetar precocemente, mas novidades nesta área não houve, diz o oncologista. “Houve um estudo há uns anos, que envolvia genómica, mas os resultados ainda são muito preliminares.”

▲ Steve Jobs, fundador da Apple, removeu o tumor pancreático em 2004. Em outubro de 2011, morreu devido à doença — Getty Images
Getty Images
É possível evitar a remoção do rim em caso de cancro?
As alterações de tratamento, sobretudo aquelas que mostram os mesmos resultados sujeitando os doentes a menos intervenções, são sempre opções a considerar. Gabriela Sousa e Paulo Cortes destacam um ensaio clínico que mostrou que os doentes com cancro do rim metastático, podiam não ter vantagens em remover cirurgicamente o órgão afetado antes de fazerem o tratamento com os antiangiogénicos.
Quando o tumor é precoce e localizado, é sempre feita a remoção do rim doente. Mas a remoção do órgão quando já existem metástases no corpo pode não trazer vantagens. A hipótese dos investigadores que apresentaram o estudo era que fosse suficiente fazer o tratamento com sunitinib, um medicamento que controla a produção de novos vasos sanguíneos, essencial à sobrevivência do cancro.
No ensaio clínico de fase III apresentado, os investigadores verificaram que os doentes com cancro de rim metastático que fizeram só tratamento com sunitinib não tiveram menos tempo de vida após o tratamento, quando comparados com os doentes que fizeram cirurgia antes do tratamento.
Há dois tipos de vantagens, para os doentes, que não fizeram a cirurgia. Por um lado, podem começar a medicação mais cedo — quatro a seis semanas mais cedo, por exemplo —, o que é importante numa situação em que o cancro pode evoluir tão rapidamente que inviabiliza o início tardio do tratamento. Por outro lado, o doente que não faz a cirurgia evita todas as complicações associadas a esta intervenção, como infeções, hemorragias, embolismos pulmonares ou problemas cardíacos.
Podemos prevenir as metástases ósseas, fraturas e recidivas com um único medicamento?
As mulheres em pós-menopausa são um grupo de risco para a osteoporose e fraturas. Um risco que se agrava no caso de mulheres que tiveram cancro da mama hormono-dependente e estão a fazer tratamento com uma classe de medicamentos chamada de inibidores de aromatase. O medicamento denosumab (dentro da classe das imunoterapias) é usado para tratar metástases ósseas e já se tinha mostrado eficaz na prevenção de fraturas. Com a vantagem de não ser revelar tóxico para as doentes. Agora, os investigadores mostraram que, nestas doentes, também previne o aparecimento de recidivas.
“Não previne as recidivas em 100% dos casos mas diminui-as de uma forma significativa e sobretudo as metástases ósseas.”, afirma Fátima Cardoso. Não foram identificadas “metástases locais ou distantes, cancro da mama na segunda mama, carcinoma secundário ou morte por outras causas”, referiu o autor do estudo Michael Gnant, investigador na Universidade Médica de Viena (Áustria).
Esta diminuição das recidivas é um efeito inesperado e acaba por funcionar como um prevenção secundária, um benefício adicional. Mas as conclusões definitivas sobre sobrevivência só poderão ser feitas após o final da experiência que ainda está a decorrer. Ainda assim, o médico David Cameron, médico na Universidade de Edimburgo (Reino Unido), não se deixou convencer. O médico não achou que fossem claros os benefícios em relação aos bifosfonatos que já são usados para prevenir os efeitos secundários dos tratamentos com os inibidores de aromatase.
Estes resultados têm implicações clínicas diretas, afirma a médica. “Já estávamos a usar um medicamento da mesma família, mas com uma injeção endovenosa [diretamente na circulação sanguínea]. Este tem a vantagem de ser subcutâneo, ser mais potente e ter menos efeitos secundários.”
Como é um medicamento destinado ao tratamento de metástases ósseas, seja qual for a origem — o cancro da próstata e do pulmão originam muitas metástases deste tipo, por exemplo —, abre-se aqui uma porta à investigação sobre os efeitos de proteção secundária que pode ser nestes casos.
E se o tratamento do cancro da mama puder ser mais curto?
O cancro da mama do subtipo HER2-positivo é dos cancros de mama mais agressivos, mas também é daqueles cujo tratamento tem mais sucesso. Está bem identificado que o gene HER2, quando mutado, leva a uma produção anormal da proteína HER2 na superfície das células. Conhecendo qual o alvo potencial de um tratamento, mais fácil é encontrar o fármaco que o combata. E assim foi.
“O HER2-positivo costumava ser dos cancros da mama mais agressivos, mas desde que existem tratamentos dirigidos passou a ser dos que melhor sabemos tratar”, conta Fátima Cardoso.
O tratamento está bem identificado, mas é caro. Em Portugal, são 30 mil euros por ano (o período de tratamento recomendado), suportados pelo Serviço Nacional de Saúde ou pelas seguradoras, refere Fátima Cardoso. “Um dos 10 medicamentos em que o Estado português gasta mais dinheiro”, acrescenta Gabriela Sousa. O que justifica o interesse do Serviço Nacional de Saúde do Reino Unido em financiar um estudo que pretendia avaliar se o tratamento feito por um período de tempo mais curto era igualmente eficaz.
O ensaio clínico de fase III envolveu mais de quatro mil mulheres com cancro da mama HER2-positivo em fase inicial e o objetivo era avaliar se seis meses de tratamento com trastuzumab tinham resultados equivalentes ao tratamento feito durante um ano. E a conclusão dos investigadores é que sim. Com a vantagem de que os efeitos secundários, nomeadamente a nível cardíaco, foram menos frequentes e mais rápidos de resolver nas doentes que fizeram apenas seis meses de tratamento.
O que são medicamentos biossimilares?
↓ Mostrar
↑ Esconder
À semelhança do que acontece com os medicamentos genéricos, os biossimilares podem aparecer no mercado depois de a patente da molécula original ter expirado.
Num e noutro caso, os medicamentos (genéricos ou biossimilares) são mais fáceis de produzir do que os originais. No entanto, no caso dos biossimilares, a produção continua a ter alguma complexidade porque se tratam de medicamentos biológicos.
Os biossimilares e os seus originais são anticorpos monoclonais produzidos com recurso a linhas celulares. Para poderem ser aprovados pelas agências do medicamento norte-americana (FDA) e europeia (EMA), os biossimilares são sujeitos a critérios mais exigentes e a controlos de qualidade maiores do que os medicamentos genéricos.
Além dos benefícios para o doente, os benefícios para os serviços de saúde são claros: com o mesmo dinheiro conseguem tratar dois doentes. Isto é particularmente importante para os países de rendimento médio, nota a médica, que desta forma poderão cumprir a recomendação da Organização Mundial de Saúde que incluiu o trastuzumab na lista dos medicamentos essenciais que todos os países devem ter para servir, pelo menos, 80% dos doentes que precisam. Fátima Cardoso alerta, no entanto, que para os países de rendimento mais baixo esta medida ainda não será suficiente. Nestes casos, os biossimilares poderão ser a solução porque são cerca de 20 a 30% mais baratos que o medicamento original. Ainda assim, a médica considera que deviam ser ainda mais baratos. “Era preciso, no mínimo, 50% de redução de preço. A competição vai acabar por conseguir isso.”
Se isto vai alterar a prática feita em Portugal e na Europa? “Para os doentes com um bom prognóstico, talvez”, diz a médica, mas sobre os restantes doentes tem mais dúvidas. “Este é o primeiro estudo neste sentido”, diz Paulo Cortes, que não vê, para já, a possibilidade de redução do tratamento. “Mas é bom olharmos e pensarmos nesta hipótese”, continua lembrando que não vai ser para todos os doentes.
“Quem escreve as recomendações europeias para o cancro da mama sou eu. Ainda vou precisar de falar com muitos colegas e ainda vai demorar algum tempo até se poder alterar as recomendações europeias”, diz Fátima Cardoso. A oncologista acredita que ainda vai haver muita discussão à volta destes resultados até que todos os médicos se sintam confortáveis em fazer o tratamento por menos tempo. “Haverá pessoas que têm receio de fazer um tratamento mais curto.”