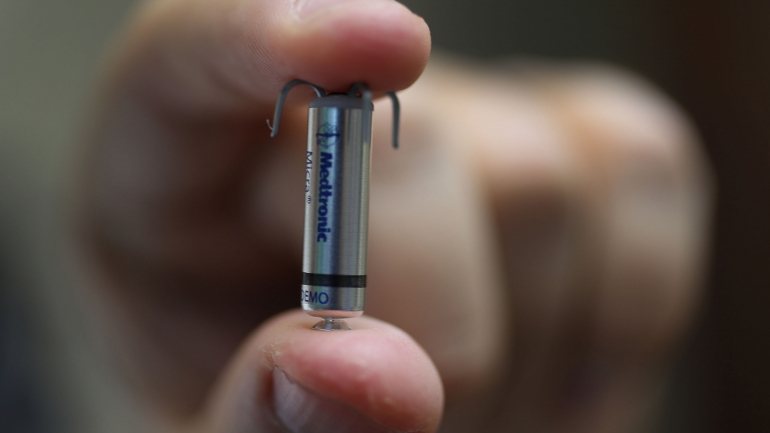
Um trabalho conjunto de mais de 250 jornalistas de 36 países denunciou que as lacunas no controlo de dispositivos médicos — como pacemakers ou implantes — provocam cada vez mais complicações, difíceis de quantificar e identificar. Só nos Estados Unidos terão provocado 1,7 milhões de lesões e cerca de 83 mil mortes na última década, noticiou o consórcio. O Infarmed garante que em Portugal “o cenário é tranquilo”.
Em França, de acordo com dados da Agência Nacional do Medicamento, o número de incidentes ligados a dispositivos médicos duplicou em dez anos, com mais de 158 mil complicações, 18 mil casos só em 2017. No Reino Unido, os reguladores receberam 62 mil queixas de incidentes com dispositivos médicos, entre 2015 e 2018, um terço dos quais tiveram repercussões graves no doente, e 1.004 resultaram em morte.
Um dos maiores problemas identificados pelo Consórcio Internacional de Jornalistas de Investigação é que os dispositivos médicos estão sujeitos a controlos de qualidade e níveis de exigência muito inferiores aos dos medicamentos. O Infarmed confirma que os dispositivos médicos não são sujeitos ao mesmo tipo de ensaios clínicos que os medicamentos porque não é possível fazer ensaios clínicos com dispositivos que impliquem um implante, como as próteses da anca. Mas que, mesmo assim, os fabricantes são obrigados a obedecer legislação específica e que cabe aos reguladores verificarem a validade das alegações. Entre os reguladores podem estar organismos estatais, como o Infarmed, ou organismos notificados, entidades não estatais que “podem ser mais permeáveis a produtos que venham de fora da Europa”, diz a autoridade do medicamento portuguesa ao Observador.
O trabalho de investigação Implant Files relatou que o lobby que têm exercido sobre os reguladores lhes tem permitido que os padrões de segurança tenham sido suavizados e que os dispositivos sejam aprovados de uma forma mais célere. Uma das preocupações é que há casos de fabricantes encarregados de testar os seus próprios produtos e que procuram aprovação pelos diversos mercados sem terem de declarar as recusas de comercialização.
Do outro lado estão os fabricantes que não têm interesse em colocar produtos no mercado que não estejam em condições. Como o caso do pacemaker que foi retirado antes de entrar no mercado porque o software podia ser alvo de ataques informáticos, exemplifica o Infarmed. A autoridade portuguesa do medicamento acrescenta ainda que em janeiro de 2019 vai entrar em vigor um novo regulamento europeu que trará regras mais apertadas para os dispositivos médicos e que pretende criar um registo dos implantes para que os doentes possam ser notificados assim que seja identificado um problema com o produto.
Entre os problemas com este tipo de produtos, o consórcio identificou perfurações nos vasos sanguíneos, choques irregulares no coração, apodrecimento dos ossos, envenenamento do sangue, entre outros problemas. Só a FDA (autoridade do medicamento norte-americana) tem registos de 5,4 milhões de “eventos adversos” relacionados com os dispositivos médicos, mas esse número pode estar muito subvalorizado. Sobretudo nos países em que esses dados não são tornados públicos ou nem sequer são registados.
A subnotificação, ou seja, a falta de denúncias dos problemas causadas por estes dispositivos às autoridades competentes é confirmada pelo Infarmed. Mas o organismo português garante que a situação em Portugal não é tão dramática como a que foi apresentada de forma global em termos internacionais. Os problemas em Portugal serão tão raros que o Infarmed, à semelhança de alguns reguladores de outros países, nem sequer chegou a ser contactado pelo consórcio.
Entre as críticas a este trabalho de investigação, o Infarmed diz que os artigos estão centrados nos casos negativos e que se perde de vista a quantidade de vidas que já foram salvas por estes tipo de dispositivos. Nenhum dispositivo médico, tal como nenhum medicamento, está isento de riscos, mas o uso desses dispositivos tem de mostrar que os benefícios compensam os riscos, diz.
Para o Infarmed também é importante referir que nem todas as mortes que estão a ser atribuídas aos dispositivos médicos, o serão de facto. As pessoas que colocam próteses, pacemakers e outro tipo de implantes já têm, na maior parte dos casos, um saúde débil e a morte pode estar relacionada com isso. Além disso, para colocar estes implantes os doentes são sujeitos a uma cirurgia que, só por si, é um fator de risco para uma morte precoce.
O consórcio admite que a ligação entre o dispositivo e uma lesão ou problema podem não ser claros, porque, tal como diz a FDA, não se podem tirar conclusões de um único evento. Mas o que este grupo fez foi agrupar todos os dispositivos de marcas diferentes e com nomes diferentes, mas que correspondem ao mesmo tipo de produto, para dar uma visão mais abrangente do problema.
As lesões causadas por alguns dispositivos também podem ser justificadas por mau uso, como pode acontecer com o uso dos preservativos contracetivos — que também são dispositivos médicos. Outro exemplo dado pelo Infarmed são as redes vaginais, não tanto pelos problemas com o produto propriamente dito, mas porque era aplicado por médicos não especializados. Em Portugal a utilização deste dispositivo é rara, confirma a autoridade do medicamento portuguesa.
O consórcio internacional de jornalistas apresenta casos de profissionais de saúde que receberam prémios de fabricantes para aconselharem os seus artigos, de produtos que foram retirados do mercado, mas só em alguns países, de produtos que os fabricantes retiraram discretamente, sem avisar as autoridades de saúde dos problemas associados ou de doentes que usaram dispositivos que, aparentemente, eram melhores, mas que depois lhes trouxeram ainda mais problemas.
Um dos exemplos é o de Maureen McCleave, uma britânica de 77 anos que colocou um pacemaker novo no mercado. Alguns dos doentes que usaram aquele pacemaker viram o músculo cardíaco perfurado, dois morreram, e em muitos outros, como Maureen McCleave, o aparelho deixou de funcionar por falta de pilha. No caso desta britânica a pilha parou ao fim de três anos quando deveria ter durado 19. Neste tipo de dispositivo, ao contrário dos aparelhos tradicionais, não é fácil de mudar a pilha. Os médicos optaram por deixar o aparelho e fazer um implante com um aparelho tradicional.