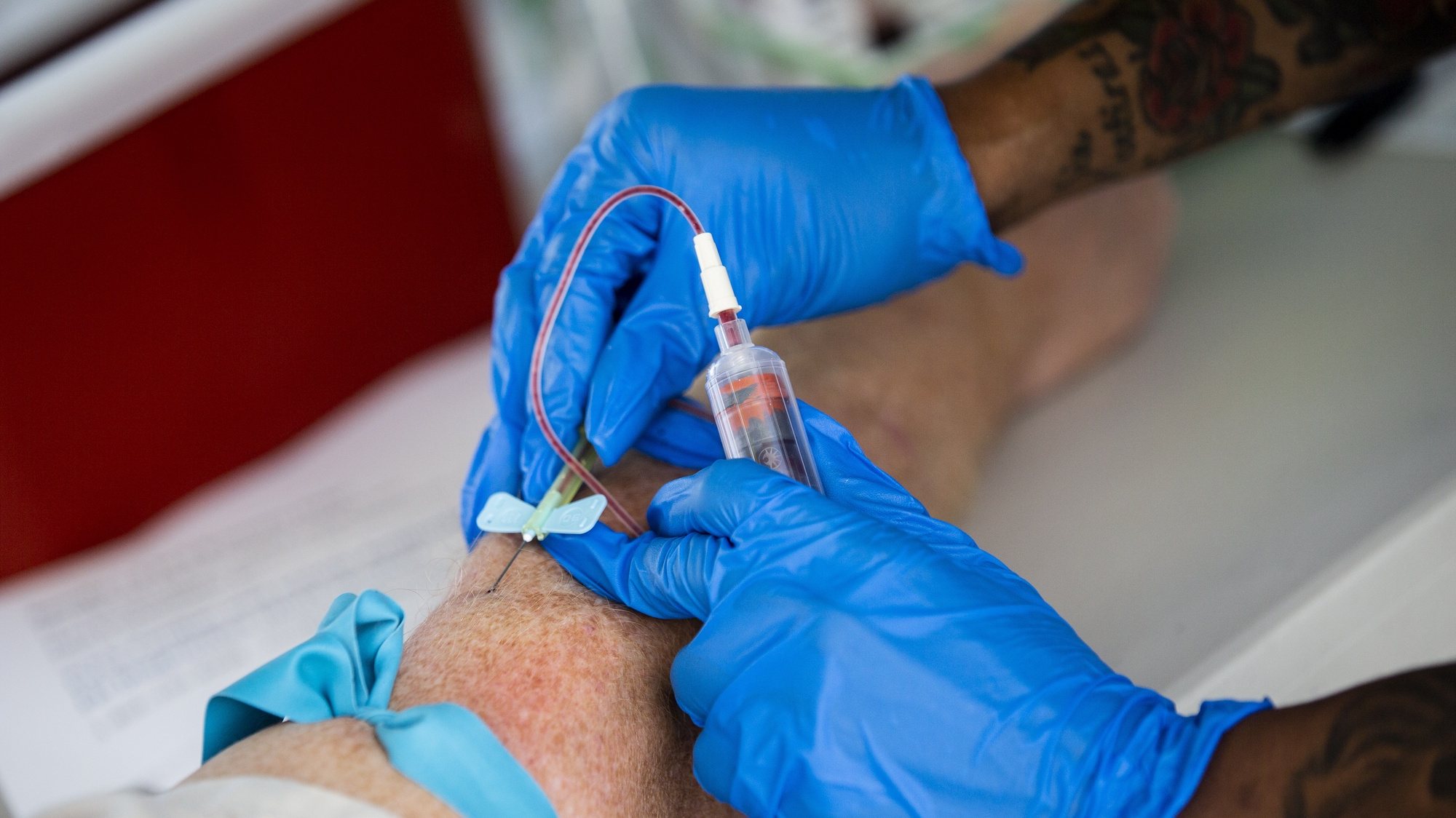
O ministro da Saúde disse esta sexta-feira, em conferência de imprensa, que o Estado português alcançou “o melhor acordo” da Europa, em relação aos tratamentos para doentes com hepatite C, com recurso aos medicamentos mais inovadores disponíveis no mercado: o Sovaldi (sofosbuvir) e o Harvoni (sofosbuvir+ledispavir). Além de ter conseguido baixar o preço por tratamento, Paulo Macedo acordou com a Gilead que só pagará caso o doente fique curado. Ou melhor dizendo, se o doente não ficar curado num tratamento, a farmacêutica terá de oferecer outro.
Com este acordo, em Portugal todos os doentes com hepatite C que necessitarem de tratamentos, estando num estadio mais ou menos avançado da doença, vão ter acesso a esta terapêutica, com uma taxa de cura superior a 95% e com efeitos secundários diminutos.
“Pensávamos tratar algumas centenas de pessoas. Neste momento vamos tratar milhares de pessoas”, afirmou o ministro da saúde, numa conferência que assinala o acordo com a farmacêutica Gilead.
Ao contrário do que se chegou a noticiar na quinta-feira, este acordo não terá a duração de três anos, mas sim de dois, até porque não faz sentido ter uma duração superior, dado que estão sempre a aparecer medicamentos novos. E o Estado propõe-se a pagar o tratamento dos 13 mil doentes reportados pelos hospitais, ainda que isso não signifique tratar efetivamente todos.
“Haverá desde logo um conjunto de pessoas que têm hepatite C, que estão registados, mas não necessitam de medicamento. 20 a 30% dos casos têm cura espontânea”, esclareceu o ministro, sem avançar contudo o número exato de doentes que será tratado nos dois anos, nem quando se chegará a esse número de 13 mil.
Fonte próxima das negociações disse ao Observador que dos 13 mil doentes reportados pelos hospitais, 7000 a 8000 vão precisar de ser medicados com estes medicamentos, porém no espaço de dois anos deverão ser tratados com estes dois fármacos entre 3000 e 5000 doentes.
Na próxima semana, um conjunto de especialistas da área, vai definir critérios para a dispensa destes fármacos. “Neste momento existe uma guideline aprovada em dezembro aprovada pela comissão de farmácia terapêutica. Vamos analisar esta guideline e ver se precisa de ser alterada e em que moldes”, esclareceu Paulo Macedo.
Estado só paga se doente ficar curado. E menos de 24 mil por doente tratado
O acordo entre o Ministério da Saúde e a Gilead, que chega ao fim de um ano de negociações, marca aqui também um momento de viragem em termos de negociações com farmacêuticas. Pela primeira vez, o Governo português conseguiu que uma empresa farmacêutica aceitasse partilhar o risco. Ou seja, caso um doente não fique curado, o laboratório oferece outro tratamento gratuito, sendo que o Governo ainda está à procura de uma metodologia para chegar ao conceito de “curado”. Além disso no acordo ficará explícito que o Estado paga por doente tratado.
“Independentemente de o doente ser tratado em oito, 12 ou 24 semanas, o Governo pagará sempre o mesmo”, esclareceu Paulo Macedo.
Embora não tenha revelado o montante acordado por tratamento, o ministro Paulo Macedo referiu que se chega “a um valor médio por doente que, como a própria Gilead disse há dois dias, é um desconto que será mais do dobro daquele que foi anunciado” inicialmente. Se no início se falava num custo por tratamento de 48 mil euros, conclui-se das palavras do governante que agora o tratamento por doente ficará abaixo dos 24 mil euros.
“Foi uma negociação difícil, mas vamos conseguir tratar mais doentes, de maneira mais equitativa, e vamos ter uma aposta na cura porque é disso que estamos a falar”, rematou o governante.
“Conseguimos gastar menos dinheiro por tratamento mas como vamos tratar mais doentes em termos do que temos previsto globalmente vamos gastar mais. Vamos gastar dezenas de milhões de euros por ano. Teremos de ter um reforço de verbas para fazer face a este encargo”, referiu Macedo.
O acordo abarca não só o acesso ao primeiro medicamento disponível desde o início de 2014 – o Sovaldi (sofosbuvir), que trata todos os seis genótipos de hepatite C – como também prevê o acesso ao novo medicamento, aprovado em dezembro na Europa – o Harvoni (sofosbuvir + ledispavir), que evita a associação com outros medicamentos, e funciona nos genótipos 1 e 4, e nalguns doentes também com genótipo 3, de acordo com a Agência Europeia do Medicamento. Ambos da Gilead Science e ambos com taxas de cura superiores a 95%.
Assim que for assinado o contrato, o que deverá acontecer na próxima semana, e definidos os critérios, será publicada uma portaria onde se estabelecerão prazos máximos de resposta para pedidos de utilização destes dois fármacos: não poderá ultrapassar os cinco dias na comissão de farmácia terapêutica do hospital, nem os dois dias no Infarmed. E então poderão ser começados a tratar os doentes com hepatite C, por ordem de emergência. O ministro acredita que ainda seja possível iniciar o novo protocolo este mês.
No final da conferência, que reuniu outros representantes da saúde como o diretor-geral de saúde, Francisco George, o secretário de Estado da Saúde, Manuel Teixeira, e responsáveis da Gilead em Portugal, o presidente do Infarmed, Eurico Castro Alves, referiu que “este será o início do inferno”, dando a entender que se seguirão negociações com outros medicamentos, de outras doenças. Esta negociação, nas suas palavras, mostra um “grande sentido de missão, muita resistência psicológica e muita coragem”.
Mais de 160 doentes já têm autorização para serem tratados com sofosbuvir e combinações
De acordo com os dados avançados pelo Infarmed, à data de ontem (5 de fevereiro) já havia 168 doentes com hepatite C com um pedido de utilização do sofosbuvir aprovado pela Autoridade do Medicamento. Resta porém saber se todos esses doentes já estavam a receber o tratamento, um levantamento que nem o Infarmed, nem o Ministério da Saúde têm, e que já pediram aos hospitais com a maior celeridade.
Até ontem o Infarmed tinha ainda aprovado 331 tratamentos com medicamentos equivalentes, seja através de ensaios clínicos (170), seja através de acesso sem custos para o SNS (161), que acontece no caso de medicamentos que já estão aprovados pela Agência Europeia do Medicamento, mas que ainda não estão a ser comparticipados em Portugal, ou ainda nem sequer fizeram pedido de introdução de preço ao Infarmed (como é o caso dos medicamentos da AbbVie e da Bristol, por exemplo). Destes 331 fazem também parte os 100 tratamentos oferecidos pela Gilead e cujo processo de entrega “termina hoje”, garantiu o presidente do Infarmed, Eurico Castro Alves, presidente do regulador do medicamento. Alguns hospitais já deram mesmo “início concreto a tratar os seus doentes”.
Em setembro do ano passado, e perante a dificuldade em estabelecer um acordo com a empresa farmacêutica, o Estado português anunciou um “plano de emergência”, que previa o tratamento de 150 doentes mais urgentes até ao final do ano com recurso a este medicamento mais inovador, e um gasto de 100 milhões de euros ao longo de cinco anos com esta terapêutica. Esse plano de emergência prolongar-se-á apenas por mais uns dias até ficarem completamente definidos os critérios para tratar os doentes, no âmbito do novo acordo.