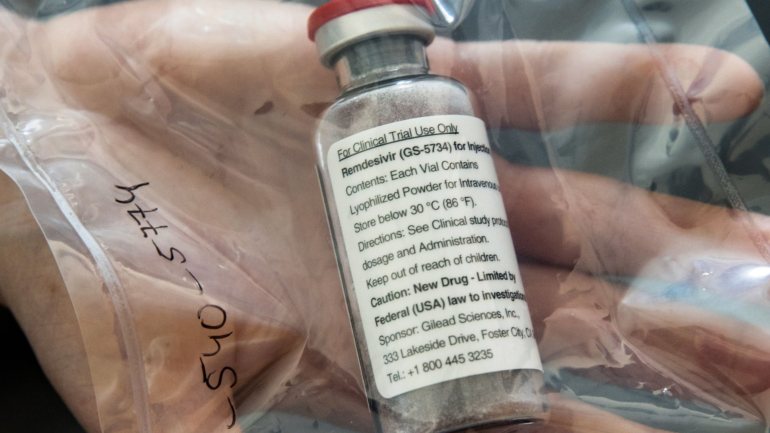
A Agência Europeia dos Medicamentos anunciou esta segunda-feira ter recebido um pedido de autorização de entrada condicional no mercado da União Europeia do antiviral remdesivir para tratamento da doença Covid-19.
“A EMA (sigla em inglês) recebeu um pedido de autorização para a entrada condicional do medicamento antiviral remdesivir para o tratamento da Covid-19 e começou oficialmente a sua avaliação”, declarou a agência em comunicado.
A avaliação das vantagens e dos riscos do remdesivir será feita num prazo reduzido e um aviso poderá ser emitido “dentro de algumas semanas”, em função da solidez dos dados submetidos e da necessidade ou não de serem fornecidas informações suplementares para a avaliação.
Nos Estados Unidos, a agência de medicamentos (FDA) autorizou a 1 de maio a utilização em urgência do remdesivir nos hospitais, seguidos do Japão, enquanto a Europa encara uma decisão semelhante.
Inicialmente desenvolvido em vão contra a febre hemorrágica do Ébola, o remdesivir, desenvolvido pelo laboratório americano Gilead, foi a primeira terapia a demonstrar uma certa eficácia nos doentes hospitalizados com Covid-19 num ensaio clínico de dimensão significativa, mesmo sendo o efeito considerado modesto.
A EMA anunciou recentemente o desenvolvimento de uma investigação independente para preparar a vigilância de eventuais vacinas contra a doença, após a sua entrada no mercado europeu.
Para autorizar qualquer vacina contra a Covid-19, a EMA tem de dispor de provas sólidas de ensaios clínicos sobre a iniquidade, a eficácia e a qualidade da vacina, indicou a agência. A EMA estimou em meados de maio que uma vacina contra o novo coronavírus poderia estar pronta dentro de um ano, num cenário “otimista”.
A pandemia de Covid-19 já provocou mais de 403 mil mortos e infetou mais de sete milhões de pessoas em 196 países e territórios, segundo o balanço feito pela agência francesa AFP. Em Portugal, morreram 1.485 pessoas das 34.885 confirmadas como infetadas, de acordo com o boletim mais recente da Direção-Geral da Saúde.