Vários estados brasileiros, a Agência Nacional de Vigilância Sanitária (Anvisa) e as instituições russas estão em desacordo. A Anvisa (regulador brasileiro dos medicamentos) acusa o Instituto Gamaleya (da Rússia) de não prestar as informações necessárias e os produtores da vacina de falhas de qualidade. Os fabricantes dizem que não é verdade e ponderam processar a Anvisa por difamação. Em causa estão as infeções causadas por esta vacina, não a sua gravidade, mas o que as causa. Mas os brasileiros só querem ter acesso à vacina rapidamente. Entre a ciência e a política, qual é, afinal, o problema com a vacina Sputnik V?
O problema com os vírus replicantes
Pelo menos 10 estados brasileiros pediram ao regulador nacional que aprovasse a importação da vacina russa, mas o pedido foi rejeitado. A Anvisa alegou que os lotes de vacinas continham adenovírus replicantes. O Instituto Gamaleya recusou a acusação. O regulador brasileiro diz que não recebeu informação atempadamente e tinha de dar uma resposta até 28 de abril por ordem do Supremo Tribunal Federal, o instituto russo só terá disponibilizado mais informação depois de conhecida a decisão.
Amilcar Tanuri, virologista da Universidade Federal do Rio de Janeiro (UFRJ), que foi contactado pelo consórcio do Nordeste (que junta nove estados brasileiros) para uma avaliação independente, diz que é possível que o problema esteja relacionado com as diferenças entre agências reguladoras. A Anvisa, do Brasil, segue os padrões de exigência da FDA, nos Estados Unidos, não admitindo vírus replicantes nas vacinas, enquanto a agência russa admite uma maior quantidade de vírus replicantes, num limite dezenas de vezes acima dos padrões internacionais.
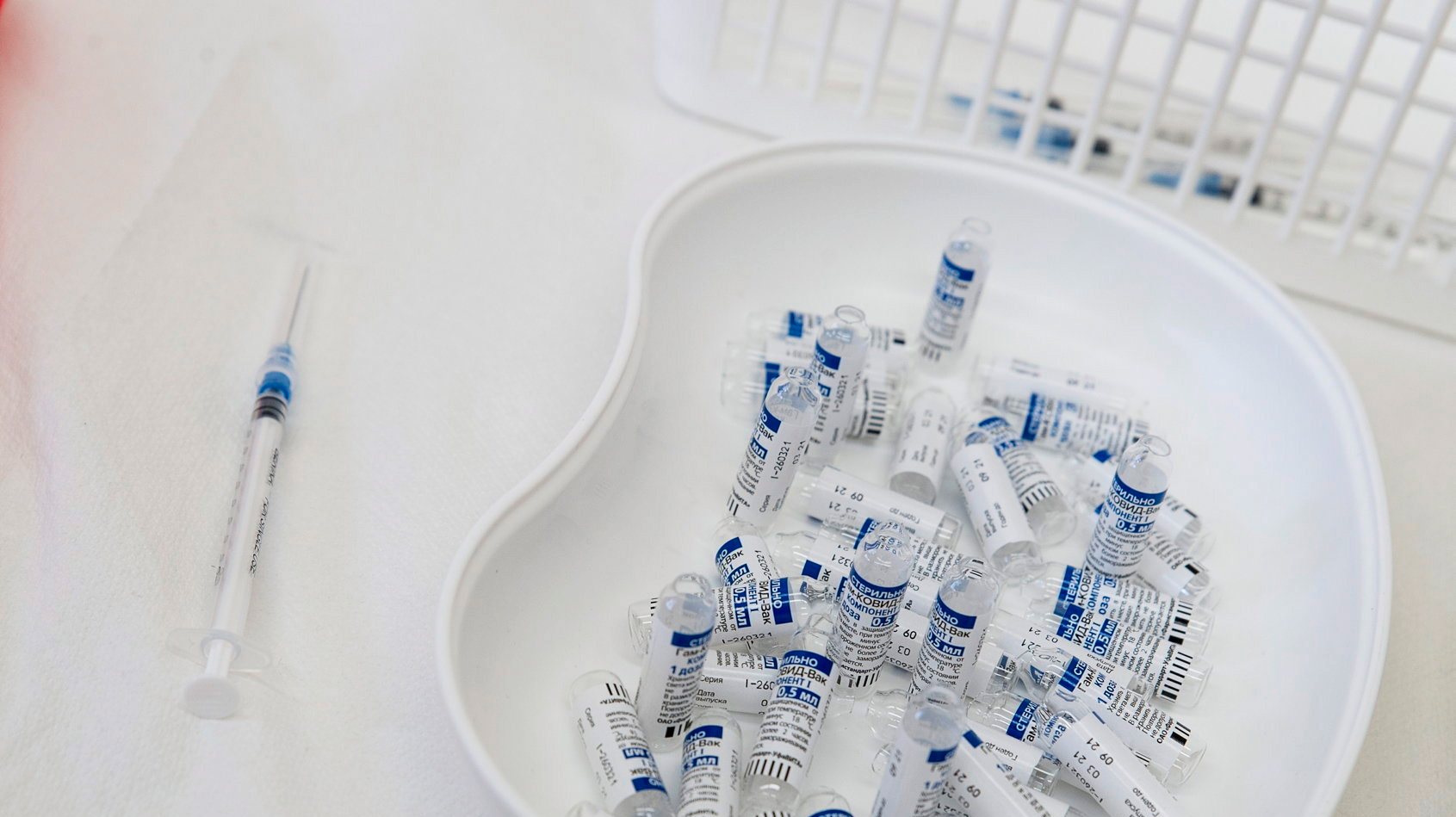
A vacina Sputnik V, como as vacinas da AstraZeneca e da Johnson & Johnson, utilizam vetores virais (ainda que diferentes entre si), ou seja, vírus que funcionam como um meio de transporte de partes do genoma do coronavírus SARS-CoV-2 para dentro das células humanas. A ideia é que as células humanas produzam a proteína spike do coronavírus. Este processo não causa infeção, mas o sistema imunitário reconhece a proteína como um agente estranho e desenvolve anticorpos e outras formas de o combater.
Covid-19. Brasil recusa vacina russa “por falta de dados consistentes e confiáveis”
A vantagem de usar vetores virais, neste caso adenovírus, é que estes já possuem estratégias para entrar dentro das células humanas — causam, por exemplo, as vulgares constipações. Aos adenovírus modificados usados nas vacinas, porém, foi-lhes retirada a capacidade de se multiplicarem. Ou seja, continuam a conseguir entrar dentro das células humanas e cumprir a sua função de transporte, mas não conseguem replicar-se e espalhar-se no organismo (daí se chamarem vetores virais não replicantes). Se não se multiplicam, também não causam doença (as tais constipações).
A acusação que recai sobre a vacina Sputnik V é que as doses contêm mais vírus com capacidade replicante do que seria desejável, ou seja, adenovírus que readquiriram a capacidade de se multiplicar e causar uma infeção (uma constipação não relacionada com o SARS-CoV-2). A Anvisa esclarece que não fizeram testes às vacinas, mas que a informação foi fornecida pelo produtor da vacina e que os próprios cientistas russos terão admitido que os técnicos do regulador brasileiro poderiam ter razão nas questões levantadas, reportou a BBC Brasil.
A infeção não é o mais grave, mas levanta outros problemas
O desenvolvimento de sintomas relacionados com a infeção com os adenovírus — que deviam ser só transporte, mas adquiriram a capacidade de se replicar — não é, só por si, muito grave: a maior parte das pessoas recupera das constipações sem problemas de maior, referiu Jorge Kalil, professor de Imunologia Clínica da Faculdade de Medicina da Universidade de São Paulo, citado pela CNN Brasil. Mas destaca: “A Anvisa tem razão em querer saber quantos existem e qual é o limite que será usado para que não se fique causando resfriado à toa ou para que não se fique causando outro problema qualquer”.
A constipação causada pelo adenovírus — desde que não seja em pessoas com o sistema imunitário fragilizado — também é minimizada se a vacina for dada no músculo e não sob a pele ou diretamente na circulação sanguínea. Ainda assim, a Anvisa ficou sem saber quanto tempo o adenovírus pode permanecer no organismo, que quantidade pode estar presente nas vacinas ou que órgãos pode afetar, referiu a Globo.
Mas pior do que a constipação (o tal ‘resfriado’), é a potencial perda de eficácia da vacina. Porquê? Com a replicação do adenovírus, o sistema imunitário vai criar defesas contra este vírus (que causa a constipação) impedindo-o de entrar nas células como é o objetivo da vacina e, potencialmente, boicotando a resposta imunitária contra o coronavírus, explicou o presidente da Sociedade Espanhola de Imunologia, Marcos López Hoyos, citado pelo jornal El Confidencial.
Outro problema, que tem ensombrado a vacina russa desde a sua aprovação — foi a primeira a ser aprovada pelo governo russo, mesmo sem terem sido divulgados publicamente os dados de eficácia — é a escassez de informação. E também foi isso que reforçou a rejeição do pedido feito à Anvisa.
Sputnik V: o que já se sabe sobre a primeira vacina da Covid-19 que Putin acaba de anunciar
“Por falta de dados consistentes e confiáveis, a Diretoria Colegiada da Anvisa decidiu, por unanimidade, não autorizar a importação em caráter excecional da vacina russa Sputnik V”, lê-se no site do Ministério da Saúde brasileiro. “A Agência é conhecida por viabilizar o acesso a medicamentos e vacinas e, neste momento de pandemia, a instituição tem atuado no limite, mas não há flexibilização em relação à segurança dos produtos.”
A equipa técnica da gerência-geral de Medicamentos e Produtos Biológicos (GGMED) verificou que existiam “falhas no desenvolvimento do produto, em todas as etapas dos estudos clínicos (fases 1, 2 e 3)”. Além disso, apontou também a “ausência ou insuficiência de dados de controlo de qualidade, segurança e eficácia”, nomeadamente porque as células usadas na produção do adenovírus que depois será usado como transporte, permitiriam a replicação do vírus. Mais, durante a visita à Rússia pela equipa de Fiscalização e Inspeção Sanitária “não foram identificadas condições de fabricação que demonstrassem que os produtos são consistentemente fabricados e controlados”.
Além disso, foram detetados estudos de caracterização inadequados da vacina, inclusive com relação à análise de impurezas e de vírus contaminantes durante o processo de fabricação, além de ausência de validação/qualificação de métodos de controlo de qualidade, entre diversos outros aspetos”, lê-se no site do Ministério da Saúde brasileiro.
Foi esta mesma incongruência entre a vacina sobre a qual foram feitos os ensaios e publicadas conclusões e as doses que foram entregues, que levaram a Eslováquia a travar a vacinação com a Sputnik V — e a uma troca de acusações entre autoridades eslovacas e russas. A Eslováquia disse que as vacinas não são idênticas e a Rússia acusou o país de não usar laboratórios autorizados para fazer as análises e exigiu as vacinas de volta.
As questões políticas e as acusações de desinformação
A primeira reação da equipa que desenvolveu a vacina da Sputnik V à decisão do regulador brasileiro foi: “A decisão da Agência Nacional de Vigilância Sanitária (Anvisa) de adiar a aprovação da Sputnik V é, infelizmente, de natureza política e nada tem a ver com o acesso do regulador à informação ou ciência”, conforme declaração oficial.
Esta opinião é apoiada pelo ex-ministro da Ciência e Tecnologia do Brasil, Sergio Rezende, que também é o coordenador científico do Consórcio Nordeste — o grupo de nove estados que viu o pedido de importação rejeitado —, segundo noticiou a DW.
A Anvisa, tal como acontece com outros medicamentos, não testou os lotes das vacinas, mas analisou os dados que foram fornecidos pelo fabricante e que incluíam limites máximos muito acima do que a agência brasileira está disposta a aceitar. O Instituto Gamaleya reforça que apesar dos limites admitidos pelo regulador russo, nenhum vetor viral replicante foi detetado e que, como tal, vai avançar com um processo judicial por difamação. A Anvisa não conseguiu confirmar este controlo de qualidade.
“O Instituto Gamaleya esclareceu à Anvisa que o limite utilizado para o controlo de qualidade da vacina Sputnik V é muito mais rígido do que o limite regulatório permitido na Rússia e corresponde aos mais rígidos padrões dos reguladores mundiais”, lê-se num comunicado da equipa que desenvolveu a vacina, emitido depois da agência brasileira comunicar a sua decisão.
Após a admissão do regulador brasileiro Anvisa de que não testou a vacina Sputnik V, a Sputnik V está iniciando um processo judicial de difamação no Brasil contra a Anvisa por espalhar informações falsas e imprecisas intencionalmente.
— Sputnik V (@sputnikvaccine) April 29, 2021
A conta do Twitter dedicada à vacina Sputnik V é bastante ativa e reporta todas as entregas da vacina nos mais de 60 países que já aprovaram o seu uso, destacando que não terão encontrado problemas nos dados fornecidos pelo instituto. Na mesma conta, há críticas àquilo a que o Fundo Russo de Investimento Direto, que patrocinou a vacina, chama de propaganda contra a vacina russa, especialmente pela União Europeia e Estados Unidos.
Esta estratégia de acusar os países e autoridades de desinformação ou de tentarem prejudicar a vacina russa foi apontada pela União Europeia como uma das formas de propagação de desinformação pró-Kremlin que cresceu desde o final do ano passado, envolvendo autoridades estatais, empresas e órgãos de comunicação afetos ao regime. “Desde o início de 2021, mais de 100 novos exemplos de alegações de desinformação pró-Kremlin sobre vacinação foram adicionados ao banco de dados da EUvsDisinfo”, lê-se no site do organismo europeu que mapeia a desinformação.
Neste contexto, os meios de comunicação pró-Kremlin, incluindo a conta oficial do Twitter da Sputnik V, têm procurado minar a confiança do público na Agência Europeia de Medicamentos e lançar dúvidas sobre seus procedimentos e imparcialidade política”, concluiu o relatório.
A acusação de falta de informação também foi levantada pela República Checa levando, também, a que a Rússia dissesse que haveria motivações políticas devido às tensões entre os dois países. A chefe do Instituto Estatal de Controlo de Drogas (SUKL), Irena Storova, disse que o organismo que dirige não recebeu documentação suficiente para fazer a avaliação da eficácia e segurança da vacina. “O que vimos é uma fração da documentação que deveria ser fornecida para o registo de uma vacina ou medicamento”, disse, citada pela DW.
A Agência Europeia do Medicamento (EMA) está a avaliar os dados da vacina Sputnik V desde março sem ter ainda resposta sobre a aprovação ou não da mesma. Jaime Pérez Martín, especialista da Associação Espanhola de Vacinologia, disse, citado pelo El Confidencial, que a EMA tem tido dificuldades no acesso aos locais onde a vacina é produzida — uma limitação também apontada pela Anvisa.
Do lado do regulador brasileiro, este não é um não definitivo. Novas avaliações com mais dados podem levar a um desfecho diferente. Existe, por exemplo, um pedido independente de autorização do laboratório União Química, uma farmacêutica brasileira que pode fabricar a Sputnik V e quer autorização de uso de emergência para o poder fazer. Caso a autorização seja dada a este laboratório brasileiro, podem ser exigidos controlos de qualidade que a Anvisa não conseguiu assegurar por parte das instituições russas.